O que é nitrogênio?
O nitrogênio (N) é um dos principais elementos que compõem os organismos vivos, juntamente com o carbono, o oxigênio e o hidrogênio. Em média, representa 2,5 a 3,5% da matéria orgânica seca nos animais. Os aminoácidos, que são os blocos estruturais das proteínas, são compostos por um grupo amina (-NH2) que contém nitrogênio e um grupo ácido carboxílico (-COOH). O nitrogênio é, portanto, o terceiro elemento mais abundante nos aminoácidos, depois do carbono (50-55%) e do oxigénio (20-23%). O nitrogênio é, portanto, essencial para o metabolismo adequado, a síntese de proteínas e, consequentemente, o crescimento animal.
1. Necessidades proteicas, metabolismo e emissões de nitrogênio na aquicultura
25 a 40%
Estas são as necessidades médias de proteína alimentar das espécies aquacultas.
As espécies aquícolas geralmente apresentam necessidades proteicas mais elevadas do que outros animais de produção, como as aves (15-22%) (Applegate e Angel, 2014). Estas necessidades mais elevadas de aminoácidos explicam-se pelo facto de que a oxidação dos aminoácidos ser a principal fonte de energia dos peixes (Weber e Haman, 1996). As necessidades proteicas alimentares dos peixes variam de acordo com a espécie e a dieta, variando entre cerca de 25-35% para espécies omnívoras e herbívoras, como a tilápia e a carpa, e 35-40% para espécies carnívoras, como os salmões, o robalo e a dourada.
As proteínas ingeridas pelos animais são rapidamente hidrolisadas em aminoácidos no trato digestivo pela ação de várias enzimas específicas: as pepsinas primeiro decompõem as proteínas em peptídeos, e posteriormente a tripsina e a quimotripsina convertem os peptídeos em aminoácidos (Engrola et al., 2009; Gamboa-Delgado et al., 2011). Esses aminoácidos são então absorvidos pelas células intestinais e usados para sintetizar novas proteínas ou para produzir energia por meio da desaminação (Bröer, 2008). O grupo amina é convertido em amônia (NH3), um resíduo metabólico que é tóxico para os animais se acumulado (Forster e Goldstein, 1969). Os organismos aquáticos podem excretar rapidamente o NH3 na água através das suas brânquias, evitando assim a sua conversão e conservando energia em comparação com animais ureotélicos, como mamíferos e aves (Figura 1).
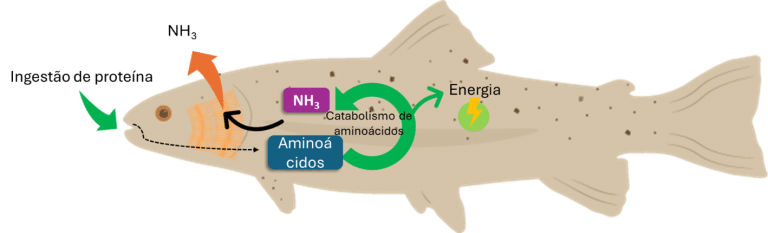
Figura 1: Metabolismo proteico e excreção de nitrogênio
(Evans et al., 2013; Weihrauch and O’Donnell, 2015)
2. O ciclo do nitrogênio e as suas várias formas na água
Uma vez libertado na água, o NH3 dilui-se facilmente. Dependendo dos parâmetros da água, principalmente o pH e a temperatura, a forma dominante será o NH3 ou o amônio (NH4+), uma forma menos tóxica para peixes e camarões, ao capturar um ião H+ (Thurston e Russo, 1983). Em pH ácido, a forma dominante é NH₄⁺, enquanto em pH alcalino (>8,5), a forma mais prevalente é NH₃. A temperatura também influencia a ionização do NH₃, com temperaturas mais altas favorecendo a forma NH₃ em detrimento da NH₄⁺
8.5
Este é o pH que não deve ser ultrapassado para limitar a formação de NH₃
Nitrificação
É o processo biológico que transforma NH₃ em NO₂⁻ e depois em NO₃⁻ através da ação de bactérias
Em seguida, o processo biológico de nitrificação transforma o NH3 em nitrato (NO3–) sob a ação de microrganismos. A nitrificação é dividida em duas etapas distintas: nitrosação e nitração, cada uma realizada por microrganismos diferentes. A nitrosação, realizada por bactérias dos géneros Nitrosomonas, Nitrosococcus e Nitrosospira, converte o NH3 em nitrito (NO2–). A nitração, realizada em particular pelos géneros Nitrobacter, Nitrococcus e Nitrospira, transforma NO2– em nitrato (NO3–). A oxidação de NH3 e NO2– fornece às bactérias a energia necessária para converter CO2 em matéria orgânica (Figura 2).
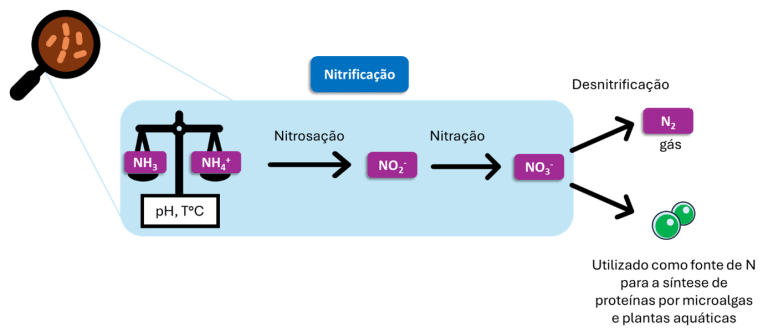
Figura 2: Ciclo do nitrogênio na água
(Robles-Porchas et al., 2020)
Para otimizar a nitrificação, é crucial manter um pH neutro, boa oxigenação e equilíbrio redox nos viveiros de peixes e camarões (Molins-Legua et al., 2006). O NO3– produzido pela nitrificação é então absorvido e utilizado como fonte de nitrogênio pelas plantas aquáticas e algas, que reduzem o NO3– a NH4+ para sintetizar aminoácidos e proteínas. Qualquer interrupção no ciclo do nitrogênio pode afetar negativamente o desempenho e a sobrevivência de peixes e camarões, gerando compostos tóxicos de nitrogênio, reduzindo a concentração de oxigênio (O2) e alterando o pH da água.
- Em trutas do lago (Salvelinus namaycush), a exposição a 198 µg/L de amônia durante 60 dias reduz a eficiência proteica em 7% (Beamish e Tandler, 1990).
- Alevinos de truta-arco-íris (Oncorhynchus mykiss) expostos a 13 mg/L de amônia durante 90 dias após a eclosão tiveram seu peso reduzido em 54% e sua taxa de sobrevivência em 70% (Brinkman et al., 2009).
- Em camarões-brancos (Litopenaeus vannamei), o acúmulo de nitrito e amônia provenientes de fezes e restos de alimento durante 33 dias reduz a taxa de sobrevivência em 2,5 vezes e a taxa de crescimento em 20,5% (Han et al., 2017).
- Em bagres-do-rio (Ictalurus punctatus), a exposição a 3,71 mg/L durante 31 dias reduz o crescimento em 20% (Colt et al., 1981).
3. Efeitos nocivos do nitrogênio na água sobre os animais aquáticos
O nitrogênio liberado na água pode afetar os animais aquáticos direta ou indiretamente. As diferentes formas de nitrogênio descritas acima, incluindo NH3, NH4+, NO2– e NO3–, apresentam níveis distintos de toxicidade para peixes e camarões. Embora as concentrações-limite na água para os diversos compostos de nitrogênio variem conforme a espécie, a ordem de toxicidade permanece a mesma para todas: NH3 é o mais tóxico, seguido por NO2–, depois NH4+ e, por último, NO3– (Figura 3).
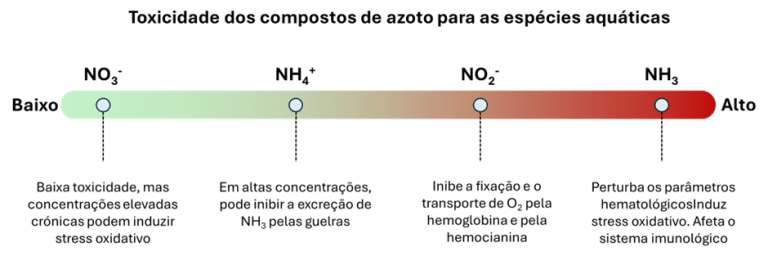
Figura 3: Toxicidade dos compostos de nitrogênio para espécies aquáticas
(Lin et al., 2023; Tomasso, 1994)
a. Toxicidade direta do nitrogênio
Como o NH3 é uma molécula não carregada, ele pode difundir-se facilmente através das membranas biológicas, especialmente das brânquias (Klocke et al., 1972; Randall e Wright, 1987). Uma vez no sangue, ele altera diversos parâmetros hematológicos, incluindo o equilíbrio ácido-base, a coagulação e o transporte de moléculas. Em peixes, o acúmulo de NH3 compromete o sistema imunológico, induz estresse oxidativo e causa danos aos tecidos das brânquias, fígado, rins e intestinos. Em crustáceos, o NH3 também induz estresse oxidativo e afeta o sistema imunológico inato e a muda (Bouwman et al., 2011; Chang et al., 2015; Cui et al., 2017; Hong et al., 2007; Rodríguez-Ramos et al., 2008; Romano e Zeng, 2013).
- Imunossupressão
- Estresse oxidative
- Neurotoxicidade
- Estresse nas brânquias
O NO₂⁻ é menos tóxico que o NH₃, mas sua toxicidade continua muito elevada. Em peixes, o principal mecanismo da toxicidade do NO₂⁻ é a formação de meta-hemoglobina (MetHb) por meio da oxidação do ferro (Fe) na hemoglobina. A MetHb não consegue mais se ligar nem transportar O₂, causando hipóxia apesar da água estar oxigenada (Jensen, 2003). Um fenômeno semelhante é observado em camarões: o NO₂⁻ oxida o cobre (Cu) na hemocianina, impedindo a ligação do O₂. O NO₂⁻ também pode induzir estresse oxidativo e comprometer o sistema imune inato de peixes e camarões. Além disso, o NO₂⁻ afeta a biologia e a saúde das brânquias (Svobodová et al., 2005), reduz a ingestão de alimento em peixes e camarões (Ribeiro-de-Campos et al., 2021; Roques et al., 2013) e prejudica seu crescimento (Ciji e Akhtar, 2020; Colt et al., 1981; Frances et al., 1998; Koo et al., 2005; Mallasen e Valenti, 2006; Siikavuopio e Sæther, 2006).
O NH4+ é muito menos tóxico, e suas concentrações na água precisam ser muito altas para afetar os animais aquáticos. Em concentrações elevadas, o NH4+ pode limitar a capacidade das brânquias de excretar NH3, levando ao acúmulo de NH3 em peixes e camarões. O NH4+ também substitui o potássio (K+) nos transportadores de íons, afetando o gradiente eletroquímico do sistema nervoso central (Cooper e Plum, 1987) e prejudicando a função cerebral (Ip e Chew, 2010).
O NO3– apresenta baixa toxicidade aguda, mas pode ter efeitos crônicos significativos. O NO3– pode causar estresse oxidativo que, se crônico, pode enfraquecer o sistema imunológico, afetar a reprodução e reduzir o crescimento. Sua toxicidade depende da concentração e do tempo de exposição (Pierce et al., 1993; Scott e Crunkilton, 2000), além da salinidade (Dowden e Bennett, 1965).
b. Impactos indiretos das emissões de nitrogênio
Quando a descarga de nitrogênio na água é excessiva, as bactérias nitrificantes podem ser sobrecarregadas pelas altas concentrações de NH3 e NO2–, fazendo com que esses compostos se acumulem na água. O excesso de nitrogênio estimula o crescimento e a proliferação de microalgas, levando à formação de florações algais. A alta concentração de microalgas reduz a penetração da luz na coluna d’água, causando sua morte. A decomposição dessa matéria orgânica pelas bactérias consome grandes quantidades de O₂, reduzindo sua concentração na água (Huo et al., 2013; Moss et al., 2013). Esse fenômeno é chamado de eutrofização (Figura 4).
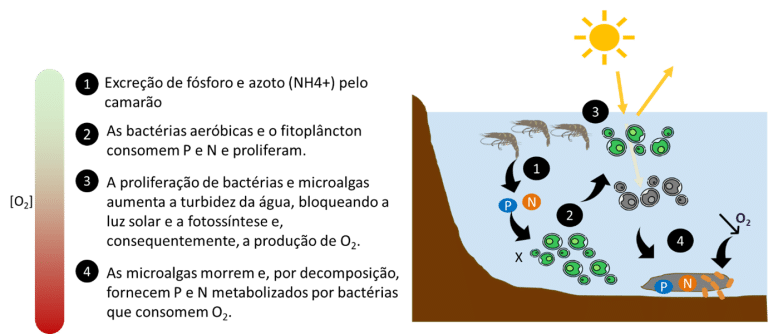
Figura 4: O processo de eutrofização
(Yang et al., 2008)
A eutrofização inicia um ciclo vicioso, em que a falta de O₂ na água provoca a morte de outros organismos aquáticos, gerando mais matéria orgânica e reduzindo ainda mais a concentração de O₂ (Yang et al., 2008). Isso tem um impacto sério no crescimento e na sobrevivência de peixes e camarões, especialmente em viveiros, que são sistemas fechados com pouca renovação de água. Em particular, observou-se que florações de algas em viveiros de camarão no México, causadas pelo excesso de nutrientes, levaram a uma taxa de mortalidade de 79,5% entre as pós-larvas, além de reduzir o crescimento (Licea, 1999).
Além disso, a eutrofização pode levar à proliferação de espécies nocivas, como as cianobactérias, que frequentemente possuem metabolismo anaeróbico, o que significa que a diminuição da concentração de oxigênio na água favorece sua proliferação (Codd, 2000). Foi observado um declínio na sobrevivência de camarões peneídeos na China e no Equador devido a florações de microalgas que causam anoxia nos viveiros (Alonso-Rodríguez e Páez-Osuna, 2003). Em sistemas abertos, como gaiolas marinhas, descargas excessivas de nitrogênio podem promover a proliferação de microalgas, algumas das quais produzem toxinas (Anderson et al., 2002) ou danificam as brânquias dos peixes com suas espículas (espinhos calcários ou silicosos), podendo levar a uma mortalidade significativa em pisciculturas afetadas (Burridge et al., 2010).
Os sistemas de aquicultura de recirculação (RAS), graças à sua capacidade de controlar os parâmetros da água, são menos afetados por esses problemas. No entanto, a descarga de nitrogênio continua sendo um problema significativo, mesmo para os sistemas tecnologicamente mais avançados. Os sistemas de filtração dos RAS são muito grandes e caros para instalar. Reduzir os níveis de nitrogênio na água pode ajudar a evitar o superdimensionamento dos sistemas de filtração e, assim, limitar os custos. Além disso, a nitrificação consome a alcalinidade da água, exigindo ajustes regulares de pH (Timmons et al., 2018).
4. Os benefícios da redução da entrada de nitrogênio nos sistemas de aquicultura
É essencial controlar os níveis de nitrogênio, tanto em instalações de aquicultura fechadas (como tanques, viveiros e sistemas de recirculação) para garantir o desempenho e o bem-estar dos animais, quanto em sistemas abertos (como gaiolas marinhas e canais de corrida) para minimizar seu impacto ambiental. Isso pode ser alcançado reduzindo as emissões de nitrogênio na água ou melhorando a capacidade das bactérias nitrificantes de converter o nitrogênio. A redução das emissões de nitrogênio envolve otimizar a distribuição da ração para evitar superalimentação e ajustar a formulação da ração para limitar a ingestão de nitrogênio. Ao modular precisamente os níveis de proteína na ração em relação a outros nutrientes, é possível reduzir o catabolismo proteico e as emissões de amônia (NH₃) na água.
Isso também envolve a escolha de outras matérias-primas, como fosfatos inorgânicos para ração. É crucial escolher produtos que limitem as emissões de fósforo (P) e nitrogênio (N) para evitar seu acúmulo na água e, assim, prevenir a eutrofização. Para esse fim, o fosfato monossódico (MSP) é a melhor escolha, pois fornece P altamente digestível para peixes e camarões, enquanto reduz as emissões de N na água em comparação com o fosfato monoamônico (MAP) (Morales et al., 2018). Embora o MAP também forneça P altamente digestível, ele também fornece excesso de NH₃ que não é utilizado pelos organismos aquáticos da mesma forma que pelos ruminantes.
Assim, embora o MAP seja um fosfato eficaz para a aquicultura, ele aumenta as emissões de nitrogênio na água (Figura 5). Portanto, para fornecer uma fonte eficaz de P, reduzindo as emissões de P e N que afetam a saúde dos peixes e o meio ambiente, é preferível optar pelo MSP.
4,2kg
Esta é a redução do N dissolvido excretado na água por tonelada de peixe produzido utilizando MSP em comparação com MAP (Morales et al., 2018).
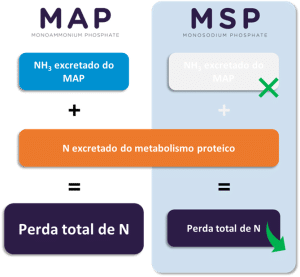
Figure 5: Redução das emissões de N com o MSP
Conclusão
O nitrogênio é um elemento essencial na aquicultura, mas seu metabolismo pode gerar resíduos tóxicos, como NH₃, quando acumulado na água. Portanto, ajustes na dieta para reduzir as emissões de N e a criação de condições ideais para as bactérias nitrificantes são necessários para minimizar os efeitos nocivos do N e garantir a saúde das espécies aquícolas. Em termos de alimentação e ingestão de P inorgânico, o MSP é a fonte mais adequada para assegurar a sustentabilidade das fazendas de aquicultura.
Bibliografia
Alonso-Rodrı́guez, R., Páez-Osuna, F., 2003. Nutrients, phytoplankton and harmful algal blooms in shrimp ponds: a review with special reference to the situation in the Gulf of California. Aquaculture 219, 317–336. https://doi.org/10.1016/S0044-8486(02)00509-4
Anderson, D.M., Glibert, P.M., Burkholder, J.M., 2002. Harmful algal blooms and eutrophication: Nutrient sources, composition, and consequences. Estuaries 25, 704–726. https://doi.org/10.1007/BF02804901
Applegate, T.J., Angel, R., 2014. Nutrient requirements of poultry publication: History and need for an update. J. Appl. Poult. Res. 23, 567–575. https://doi.org/10.3382/japr.2014-00980
Beamish, F.W.H., Tandler, A., 1990. Ambient ammonia, diet and growth in lake trout. Aquat. Toxicol. 17, 155–166. https://doi.org/10.1016/0166-445X(90)90028-N
Bouwman, A.F., Pawłowski, M., Liu, C., Beusen, A.H.W., Shumway, S.E., Glibert, P.M., Overbeek, C.C., 2011. Global Hindcasts and Future Projections of Coastal Nitrogen and Phosphorus Loads Due to Shellfish and Seaweed Aquaculture. Rev. Fish. Sci. 19, 331–357. https://doi.org/10.1080/10641262.2011.603849
Brinkman, S.F., Woodling, J.D., Vajda, A.M., Norris, D.O., 2009. Chronic Toxicity of Ammonia to Early Life Stage Rainbow Trout. Trans. Am. Fish. Soc. 138, 433–440. https://doi.org/10.1577/T07-224.1
Bröer, S., 2008. Amino Acid Transport Across Mammalian Intestinal and Renal Epithelia. Physiol. Rev. 88, 249–286. https://doi.org/10.1152/physrev.00018.2006
Burridge, L., Weis, J.S., Cabello, F., Pizarro, J., Bostick, K., 2010. Chemical use in salmon aquaculture: A review of current practices and possible environmental effects. Aquaculture 306, 7–23. https://doi.org/10.1016/j.aquaculture.2010.05.020
Chang, Z.-W., Chiang, P.-C., Cheng, W., Chang, C.-C., 2015. Impact of ammonia exposure on coagulation in white shrimp, Litopenaeus vannamei. Ecotoxicol. Environ. Saf. 118, 98–102. https://doi.org/10.1016/j.ecoenv.2015.04.019
Ciji, A., Akhtar, M.S., 2020. Nitrite implications and its management strategies in aquaculture: a review. Rev. Aquac. 12, 878–908. https://doi.org/10.1111/raq.12354
Codd, G.A., 2000. Cyanobacterial toxins, the perception of water quality, and the prioritisation of eutrophication control. Ecol. Eng. 16, 51–60. https://doi.org/10.1016/S0925-8574(00)00089-6
Colt, J., Ludwig, R., Tchobanoglous, G., Cech, J.J., 1981. The effects of nitrite on the short-term growth and survival of channel catfish, Ictalurus punctatus. Aquaculture 24, 111–122. https://doi.org/10.1016/0044-8486(81)90048-X
Cooper, A.J., Plum, F., 1987. Biochemistry and physiology of brain ammonia. Physiol. Rev. 67, 440–519. https://doi.org/10.1152/physrev.1987.67.2.440
Cui, Y., Ren, X., Li, J., Zhai, Q., Feng, Y., Xu, Y., Ma, L., 2017. Effects of ammonia-N stress on metabolic and immune function via the neuroendocrine system in Litopenaeus vannamei. Fish Shellfish Immunol. 64, 270–275. https://doi.org/10.1016/j.fsi.2017.03.028
Dowden, B.F., Bennett, H.J., 1965. Toxicity of Selected Chemicals to Certain Animals. J. Water Pollut. Control Fed. 37, 1308–1316.
Engrola, S., Mai, M., Dinis, M.T., Conceição, L.E.C., 2009. Co-feeding of inert diet from mouth opening does not impair protein utilization by Senegalese sole (Solea senegalensis) larvae. Aquaculture 287, 185–190. https://doi.org/10.1016/j.aquaculture.2008.10.036
Evans, D.H., Claiborne, J.B., Currie, S., 2013. The Physiology of Fishes, Fourth Edition. CRC Press.
Forster, R.P., Goldstein, L., 1969. 5 Formation of Excretory Products, in: Hoar, W.S., Randall, D.J. (Eds.), Fish Physiology, Excretion, Ionic Regulation, and Metabolism. Academic Press, pp. 313–350. https://doi.org/10.1016/S1546-5098(08)60086-2
Frances, J., Allan, G.L., Nowak, B.F., 1998. The effects of nitrite on the short-term growth of silver perch (Bidyanus bidyanus). Aquaculture 163, 63–72. https://doi.org/10.1016/S0044-8486(98)00219-1
Gamboa-Delgado, J., Peña-Rodríguez, A., Ricque-Marie, D., Cruz-Suárez, L.E., 2011. Assessment of Nutrient Allocation and Metabolic Turnover Rate in Pacific White Shrimp Litopenaeus vannamei Co-Fed Live Macroalgae Ulva clathrata and Inert Feed: Dual Stable Isotope Analysis. J. Shellfish Res. 30, 969–978. https://doi.org/10.2983/035.030.0340
Han, S., Wang, B., Wang, M., Liu, Q., Zhao, W., Wang, L., 2017. Effects of ammonia and nitrite accumulation on the survival and growth performance of white shrimp Litopenaeus vannamei. Invertebr. Surviv. J. 14, 221–232. https://doi.org/10.25431/1824-307X/isj.v14i1.221-232
Hong, M., Chen, L., Sun, X., Gu, S., Zhang, L., Chen, Y., 2007. Metabolic and immune responses in Chinese mitten-handed crab (Eriocheir sinensis) juveniles exposed to elevated ambient ammonia. Comp. Biochem. Physiol. Part C Toxicol. Pharmacol. 145, 363–369. https://doi.org/10.1016/j.cbpc.2007.01.003
Huo, S., Ma, C., Xi, B., Su, J., Zan, F., Ji, D., He, Z., 2013. Establishing eutrophication assessment standards for four lake regions, China. J. Environ. Sci. 25, 2014–2022. https://doi.org/10.1016/S1001-0742(12)60250-2
Ip, A.Y.K., Chew, S.F., 2010. Ammonia Production, Excretion, Toxicity, and Defense in Fish: A Review. Front. Physiol. 1. https://doi.org/10.3389/fphys.2010.00134
Jensen, F.B., 2003. Nitrite disrupts multiple physiological functions in aquatic animals. Comp. Biochem. Physiol. A. Mol. Integr. Physiol. 135, 9–24. https://doi.org/10.1016/s1095-6433(02)00323-9
Kaushik, S.J., 1998. Whole body amino acid composition of European seabass (Dicentrarchus labrax), gilthead seabream (Sparus aurata) and turbot (Psetta maxima) with an estimation of their IAA requirement profiles. Aquat. Living Resour. 11, 355–358. https://doi.org/10.1016/S0990-7440(98)80007-7
Klocke, R., Andersson, K., Rotman, H., Forster, R., 1972. Permeability of human erythrocytes to ammonia and weak acids. Am. J. Physiol.-Leg. Content 222, 1004–1013. https://doi.org/10.1152/ajplegacy.1972.222.4.1004
Koo, J.-G., Kim, S.-G., Jee, J.-H., Kim, J.-M., Bai, S.C., Kang, J.-C., 2005. Effects of ammonia and nitrite on survival, growth and moulting in juvenile tiger crab, Orithyia sinica (Linnaeus). Aquac. Res. 36, 79–85. https://doi.org/10.1111/j.1365-2109.2004.01187.x
Licea, S., 1999. Proliferaciones de microalgas nocivas en los estanques para el cultivo semi-intensivo de camarón en México. Rev. Latinoam. Microbiol. 38, 123.
Lin, W., Luo, H., Wu, J., Hung, T.-C., Cao, B., Liu, X., Yang, J., Yang, P., 2023. A Review of the Emerging Risks of Acute Ammonia Nitrogen Toxicity to Aquatic Decapod Crustaceans. Water 15, 27. https://doi.org/10.3390/w15010027
Mallasen, M., Valenti, W.C., 2006. Effect of nitrite on larval development of giant river prawn Macrobrachium rosenbergii. Aquaculture 261, 1292–1298. https://doi.org/10.1016/j.aquaculture.2006.07.048
Molins-Legua, C., Meseguer-Lloret, S., Moliner-Martinez, Y., Campíns-Falcó, P., 2006. A guide for selecting the most appropriate method for ammonium determination in water analysis. TrAC Trends Anal. Chem. 25, 282–290. https://doi.org/10.1016/j.trac.2005.12.002
Morales, G.A., Azcuy, R.L., Casaretto, M.E., Márquez, L., Hernández, A.J., Gómez, F., Koppe, W., Mereu, A., 2018. Effect of different inorganic phosphorus sources on growth performance, digestibility, retention efficiency and discharge of nutrients in rainbow trout (Oncorhynchus mykiss). Aquaculture 495, 568–574. https://doi.org/10.1016/j.aquaculture.2018.06.036
Moss, B., Jeppesen, E., Søndergaard, M., Lauridsen, T.L., Liu, Z., 2013. Nitrogen, macrophytes, shallow lakes and nutrient limitation: resolution of a current controversy? Hydrobiologia 710, 3–21. https://doi.org/10.1007/s10750-012-1033-0
Nutrient Requirements of Fish and Shrimp, 2011. . National Academies Press, Washington, D.C. https://doi.org/10.17226/13039
Pierce, R.H., Weeks, J.M., Prappas, J.M., 1993. Nitrate Toxicity to Five Species of Marine Fish. J. World Aquac. Soc. 24, 105–107. https://doi.org/10.1111/j.1749-7345.1993.tb00156.x
Pinho, S.M., Emerenciano, M.G.C., 2021. Sensorial attributes and growth performance of whiteleg shrimp (Litopenaeus vannamei) cultured in biofloc technology with varying water salinity and dietary protein content. Aquaculture 540, 736727. https://doi.org/10.1016/j.aquaculture.2021.736727
Randall, D.J., Wright, P.A., 1987. Ammonia distribution and excretion in fish. Fish Physiol. Biochem. 3, 107–120. https://doi.org/10.1007/BF02180412
Ribeiro-de-Campos, B., Ortiz-Kracizy, R., Furtado, P.S., Volkweis-Zadinelo, I., Cupertino-Ballester, E.L., Ribeiro-de-Campos, B., Ortiz-Kracizy, R., Furtado, P.S., Volkweis-Zadinelo, I., Cupertino-Ballester, E.L., 2021. Effects of ammonia and nitrite on food consumption of the Amazon River prawn Macrobrachium amazonicum (Heller, 1862) postlarvae. Lat. Am. J. Aquat. Res. 49, 684–688. https://doi.org/10.3856/vol49-issue4-fulltext-2583
Robles-Porchas, G.R., Gollas-Galván, T., Martínez-Porchas, M., Martínez-Cordova, L.R., Miranda-Baeza, A., Vargas-Albores, F., 2020. The nitrification process for nitrogen removal in biofloc system aquaculture. Rev. Aquac. 12, 2228–2249. https://doi.org/10.1111/raq.12431
Rodríguez-Ramos, T., Espinosa, G., Hernández-López, J., Gollas-Galván, T., Marrero, J., Borrell, Y., Alonso, M.E., Bécquer, U., Alonso, M., 2008. Effects of Echerichia coli lipopolysaccharides and dissolved ammonia on immune response in southern white shrimp Litopenaeus schmitti. Aquaculture 274, 118–125. https://doi.org/10.1016/j.aquaculture.2007.10.049
Romano, N., Zeng, C., 2013. Toxic Effects of Ammonia, Nitrite, and Nitrate to Decapod Crustaceans: A Review on Factors Influencing their Toxicity, Physiological Consequences, and Coping Mechanisms. Rev. Fish. Sci. 21, 1–21. https://doi.org/10.1080/10641262.2012.753404
Roques, J., Schram, E., Spanings, T., 2013. The impact of elevated water nitrite concentration on physiology, growth and feed intake of African catfish Clarias gariepinus (Burchell 1822) – Roques – 2015 – Aquaculture Research – Wiley Online Library [WWW Document]. URL https://onlinelibrary.wiley.com/doi/abs/10.1111/are.12292 (accessed 10.29.25).
Scott, G., Crunkilton, R.L., 2000. Acute and chronic toxicity of nitrate to fathead minnows (Pimephales promelas), ceriodaphnia dubia, and Daphnia magna. Environ. Toxicol. Chem. 19, 2918–2922. https://doi.org/10.1002/etc.5620191211
Siikavuopio, S.I., Sæther, B.-S., 2006. Effects of chronic nitrite exposure on growth in juvenile Atlantic cod, Gadus morhua. Aquaculture 255, 351–356. https://doi.org/10.1016/j.aquaculture.2005.11.058
Svobodová, Z., Máchová, J., Poleszczuk, G., Hůda, J., Hamáčková, J., Kroupová, H., 2005. Nitrite Poisoning of Fish in Aquaculture Facilities with Water-recirculating Systems. Acta Vet. Brno 74, 129–137. https://doi.org/10.2754/avb200574010129
Thurston, R.V., Russo, R.C., 1983. Acute Toxicity of Ammonia to Rainbow Trout. Trans. Am. Fish. Soc. 112, 696–704. https://doi.org/10.1577/1548-8659(1983)112<696:ATOATR>2.0.CO;2
Timmons, M., Guerdat, T., Vinci, B., 2018. Recirculating Aquaculture, 4th edition.
Tomasso, J.R., 1994. Toxicity of nitrogenous wastes to aquaculture animals. Rev. Fish. Sci. 2, 291–314. https://doi.org/10.1080/10641269409388560
Weber, J.-M., Haman, F., 1996. Pathways for metabolic fuels and oxygen in high performance fish. Comp. Biochem. Physiol. A Physiol. 113, 33–38. https://doi.org/10.1016/0300-9629(95)02063-2
Weerd, J.H.V., 1995. Nutrition and growth in Clarias species – a review. Aquat. Living Resour. 8, 395–401. https://doi.org/10.1051/alr:1995046
Weihrauch, D., O’Donnell, M.J., 2015. Links between Osmoregulation and Nitrogen-Excretion in Insects and Crustaceans. Integr. Comp. Biol. 55, 816–829. https://doi.org/10.1093/icb/icv013
Yang, X., Wu, X., Hao, H., He, Z., 2008. Mechanisms and assessment of water eutrophication. J. Zhejiang Univ. Sci. B 9, 197–209. https://doi.org/10.1631/jzus.B0710626
