Introducción
Los rumiantes se diferencian de otros animales por su sistema digestivo: poseen un rumen. El rumen es el principal sitio de digestión del alimento, ya que alberga microorganismos responsables de la fermentación biológica de los mismos. Así, alimentar a un rumiante es alimentar su microbiota ruminal. Los rumiantes están adaptados a digerir alimentos voluminosos y fibrosos, pero la evolución de los sistemas de producción ha transformado su dieta e incorporado materias primas con mayor valor nutricional y menor porcentaje de fibra. Esta intensificación de las dietas buscó mejorar las productividades animales y económicos del sistema, y conduce a alteraciones en el ambiente ruminal cuando no se gestionan adecuadamente. Una de las alteraciones con mayor incidencia es la acidosis ruminal subclínica (SARA, por sus siglas en inglés) caracterizada por períodos prolongados de pH ruminal debajo de un umbral (generalmente entre 5.7 o 5.5). A diferencia de la forma aguda, su sintomatología es silenciosa pero persistente, causada por un exceso de carbohidratos fermentables en la dieta o por un fallo en la formulación de la ración. La SARA es un problema recurrente, ya que está presente entre el 19% y el 26% de las vacas lecheras en producción (Kleen et al., 2013). La presencia de SARA está asociada con importantes alteraciones en la salud y el rendimiento animal, especialmente una disminución en la digestibilidad de la fibra (~10%; Orne Conseil Élevage, 2016) y una reducción de la producción de leche (~2.7 kg; Enemark, 2008)
¿Qué es la acidosis ruminal subclínica?
La acidosis ruminal subaguda (SARA) es uno de los principales problemas nutricionales en vacas lecheras. Este trastorno metabólico provoca una alteración de las fermentaciones ruminales, causada por una transición alimentaria inadecuada y/o una composición de la dieta inapropiada. La SARA resulta de un desequilibrio de la microbiota ruminal causado por una dieta rica en carbohidratos fermentables y/o pobre en proteínas, yrepresenta una amenaza constante para los rumiantes de alto nivel de producción.
El pH óptimo del rumen para las vacas lecheras de estos sistemasse sitúa entre 6 y 6.5, lo que permite un equilibrio adecuado de la microbiota ruminal. Sin embargo, debido a las estrategias de alimentación intensivas, se observan extremas fluctuaciones diarias del pH ruminal, lo que favorece una degradación del epitelio ruminal y una disminución de la capacidad de absorción de nutrientes (Figura 1). Como consecuencia, sedeteriora la salud y el rendimiento zootécnico de los animales.
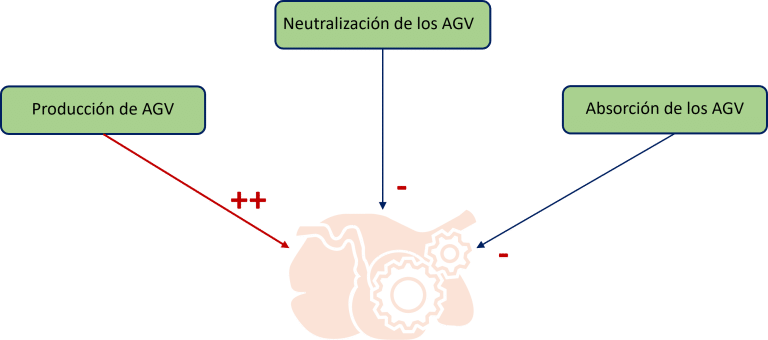
Figura 1: Origen de la acidosis subaguda.
La acidosis ruminal puede definirse como una disminución del pH ruminal cuando la producción de ácidos, en particular ácidos grasos volátiles (AGV), supera su neutralización y absorción. Existen dos formas de acidosis ruminal: la acidosis aguda y la acidosis subclínica o subaguda (Sauvant, Reverdin y Meschy, 2006). Es esta última la que se desarrolla a continuación.
La SARA es la consecuencia de un desequilibrio de la energía/proteína en la alimentación
La acidosis ruminal puede definirse como una disminución del pH ruminal cuando la producción de ácidos, en particular ácidos grasos volátiles (AGV), supera su neutralización y absorción. Existen dos formas de acidosis ruminal: la acidosis aguda y la acidosis subclínica o subaguda (Sauvant, Reverdin y Meschy, 2006). Es esta última la que se desarrolla a continuación.
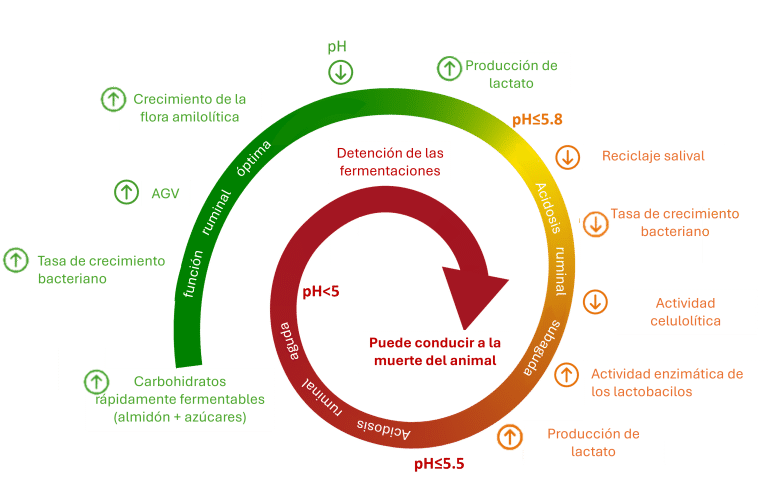
Figura 2: Círculo vicioso de la acidosis. Adaptado de Hernandez et al., 2014
Transición alimentaria: un período de alto riesgo para vacas
Las variaciones de calidad de los silos o del forraje ponen a prueba la estabilidad de la dieta. Por ejemplo, el ensilado de maíz sigue evolucionando algunas semanas después de su confección y, aúnque de una única cosecha, puede presentar variaciones semanales en sus valores nutricionales ( contenido de azúcares, digestibilidad del almidón, contenido de materia seca, etc.). En otros casos las vacas se alimentan con forrajes frescos, lo que puede desembocar en trastornos digestivos. En comparación con los forrajes conservados, los forrajes frescos son ricos en azucares de rapida fermantación, los cuales generan reacciones rápidas y desequilibradas, aumentando el riesgo de SARA en el animal y comprometiendo la estabilidad de la microbiota . Cuando estos azucares se metabolizan en rumen, la flora amilolítica se sobre-estimula y se producen grandes cantidades de AGV (en especial propionato y butirato) superando la tasa de absorción por la pared ruminal y la neutralización por la saliva.
Dificultades similares surgen con s forrajes en primavera y/o otoño. Además de contener carbohidratos de rápida fermentabilidad , son ricos en nitrógeno y pobre en fibras, que los hace muy palatable . En este sentido los animales los consumen rápidamente, disminuyendo la salivación y aumenta el riesgo de SARA. Debido a su alto contenido de bicarbonato de sodio (12.5 g/L según Erdman, 1988), la saliva constituye un tampón natural para el pH ruminal. Así, una producción de saliva reducida implica menor efecto tampón en el rumen.
Niveles y la fuente del almidón aumentan el riesgo de SARA
La composición de la dieta es un factor clave en la gestión de la SARA. Por ejemplo, el contenido de almidón, así como su origen, pueden aumentar el riesgo de SARA. Elmhadi et al. (2022) afirman que un contenido de almidón entre 50% y 65% puede inducir SARA. Khorrami et al. (2021) confirman que el tiempo pasado con un pH ruminal bajo (< 6) aumenta con el contenido de almidón de la dieta. También identificaron que el tipo de almidón utilizado puede influir en el riesgo de SARA. El almidón de maíz es más acidógenico que la cebada y el trigo cuando se suministra en grandes cantidades (> 20 % de la materia seca total; Khorrami et al., 2021).
¿Cómo detectar la SARA?
Las consecuencias de la SARA pueden ser numerosas y variar de un animal a otro. Pueden manifestarse en forma de una o más de las observaciones visuales enumeradas en la Figura 3.
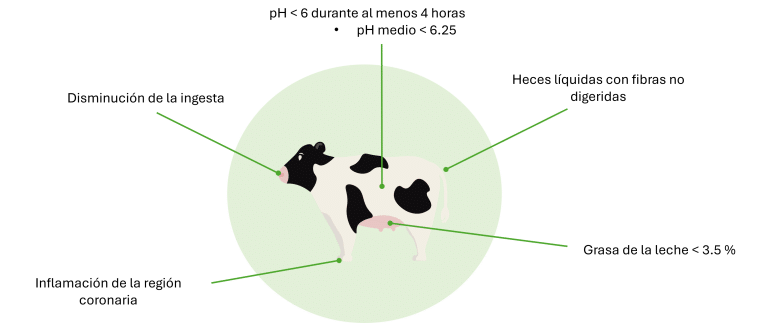
Figura 3: ¿Cómo reconocer la SARA en los animales?
Al reducir el consumo de materia seca (CMI; – 2.3 kg/día en promedio con SARA) y afectar la actividad del rumen, la SARA conduce a una disminución de la producción de leche que puede variar de 1.8 kg/día a 3.3 kg/día (Chiquette et al. 2015). Además de esta pérdida de producción, la disminución de la actividad de las bacterias celulolíticas afecta el contenido de grasa en la leche debido a una menor producción de acetato, un AGV precursor de grasa de la leche. Chiquette et al. (2015) observaron una disminución del 0.18% en el porcentaje de grasa de la leche durante un desafío de SARA. En animales jóvenes, la SARA también se asocia con una reducción de la CMS y de la ganancia de peso promedio en terneros antes del destete (Wenli Li et al., 2019). Además, la SARA puede afectar indirectamente el rendimiento reproductivo. De hecho, una menor eficiencia alimentaria puede conducir a una condición corporal insuficiente que afecta la reproducción. Como muestran Seesupa et al. (2017), la SARA también puede modificar el sistema hormonal, lo que provoca una menor fertilidad. Teniendo en cuenta todo esto, la SARA representa un costo para el ganadero que puede alcanzar 1.12 a 1.2 €/vaca/día (Plaizier et al., 2008).
¿Cómo limitar el riesgo de SARA?
Para reducir el riesgo de SARA es importante respetar los principios fundamentales de la nutrición de los rumiantes:
- Realizar transiciones alimentarias progresivas
- Proporcionar suficiente agua
- Asegurar un consumo regular de alimentos a lo largo del día
- Analizar el forraje para obtener una dieta equilibrada en energía y proteína
El perfil nutricional en términos de almidón y fibras también es muy importante. En particular, el contenido y la calidad de la fibra son esenciales para gestionar el riesgo de SARA. Como menciona Khorrami et al. (2021), los casos de SARA aumentan cuando el contenido de almidón supera el 20% y la peNDF > 8 (entendiendo peNDF como la fibra detergente neutra físicamente efectiva) es inferior al 14%.
El uso sistemático o específico de soluciones tampones durante períodos de riesgo de SARA representa una estrategia clave para apoyar a los animales y mantener una actividad ruminal óptima. En Phosphea nos comprometemos a contribuir a limitar el riesgo de SARA ofreciendo nuestra solución tampón natural: CALSEA Powder.
¿Cómo puede contribuir CALSEA Powder a la gestión de la SARA?
CALSEA Powder es una solución natural basada 100% en algas marinas calcáreas (Lithothamnium calcareum). La estructura porosa de esta alga marina, combinada con su estructura cristalina única, permite una elevada solubilización y una rápida liberación de iones de calcio y carbonato en el rumen, lo que permite un mejor mantenimiento del pH ruminal.
Las vacas que reciben el tratamiento con bicarbonato de sodio (SBC; 200 g/vaca/día) presentan un pH ruminal medio más bajo que aquellas con el tratamiento CALSEA (100 g/vaca/día; Figura 4). El pH ruminal mínimo obtenido con el tratamiento SBC es de 5.45, lo cual es significativamente inferior al pH ruminal mínimo obtenido con CALSEA (Figura 4). Además, con CALSEA, el porcentaje de animales con un pH ruminal < 5.5 es significativamente inferior al del SBC (Figura 4). Un pH < 6 durante al menos 4 horas representa un riesgo de acidosis y, cuando el pH es <5.5, este riesgo es elevado. Según los resultados, la capacidad tampón de CALSEA es superior a la del SBC.
CALSEA Powder actúa como una solución tampón favoreciendo la estabilidad del pH ruminal, con efectos positivos sobre las poblaciones microbianas ruminales y un menor riesgo de SARA. La Figura 5 muestra la abundancia relativa de ciertas bacterias indicadoras del estado de SARA con diferentes soluciones tampones.
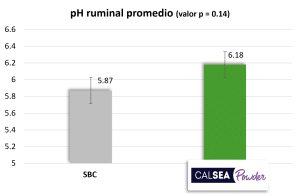
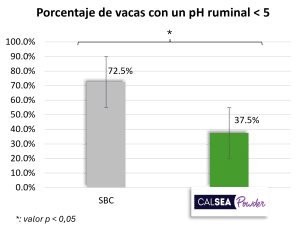
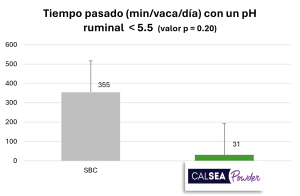
Figura 4: Acción de CALSEA Powder sobre el pH ruminal comparado al bicarbonato de sodio (ensayo en vivo ; n=40).
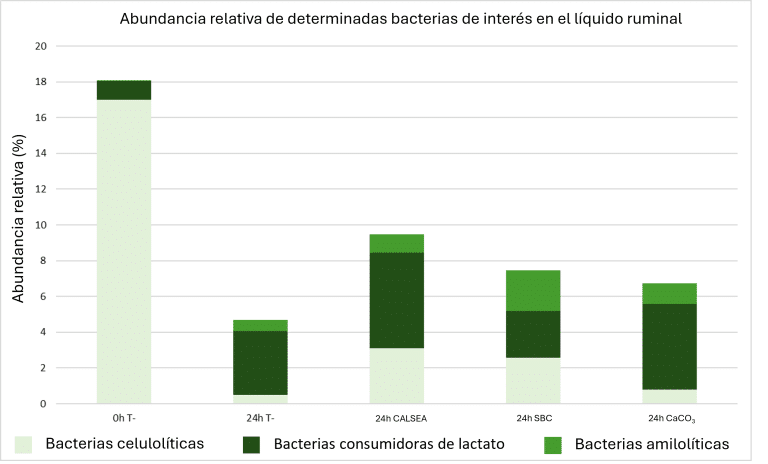
Figura 5: Seguimiento in vitro de las poblaciones bacterianas ruminales en caso de acidosis ruminal subclínica (T-: Control con SARA).
0h T- representa el control negativo sin tampón en el tiempo 0. En esta etapa, el efecto acidógeno de la dieta no es visible, la situación se considera normal. Después de 24 horas de fermentación sin tampón (24h T-) las bacterias se han afectado negativamente y en particular las celulolíticas, cuya población ha disminuido drásticamente. En comparación con el control negativo (T-24h), CALSEA (100 g/vaca/día) y SBC (200 g/vaca/día) tienden a estimular la actividad celulolítica (Fibrobacter). Por otro lado, las bacterias consumidoras de lactato (Megasphaera) están más presentes con CALSEA y CaCO3 que con SBC. Esta última bacteria protege contra la SARA porque consume el ácido láctico.
Este ensayo muestra que CALSEA favorece la actividad bacteriana celulolítica en condiciones acidógenicas, contribuyendo a mantener una eficacia ruminal óptima.
Products tailored to your livestock's need
Bibliografía
CHIQUETTE, J., LAGROST, J., GIRARD, C.L., TALBOT, G., LI, S., PLAIZIER, J.C. and HINDRICHSEN, I.K., 2015. Efficacy of the direct-fed microbial Enterococcus faecium alone or in combination with Saccharomyces cerevisiae or Lactococcus lactis during induced subacute ruminal acidosis. Journal of Dairy Science. January 2015. Vol. 98, n° 1, pp. 190‑203. DOI 10.3168/jds.2014-8219.
ELMHADI, Mawda E., ALI, Darien K., KHOGALI, Mawahib K. and WANG, Hongrong, 2022. Subacute ruminal acidosis in dairy herds: Microbiological and nutritional causes, consequences, and prevention strategies. Animal Nutrition. September 2022. Vol. 10, pp. 148‑155. DOI 10.1016/j.aninu.2021.12.008.
ENEMARK, Jörg M. D., 2008. The monitoring, prevention and treatment of sub-acute ruminal acidosis (SARA): A review. The Veterinary Journal. April 2008. Vol. 176, n° 1, pp. 32‑43. DOI 10.1016/j.tvjl.2007.12.021.
ERDMAN, Richard A., 1988. Dietary Buffering Requirements of the Lactating Dairy Cow: A Review1. Journal of Dairy Science. December 1988. Vol. 71, n° 12, pp. 3246‑3266. DOI 10.3168/jds.S0022-0302(88)79930-0.
FAOSTAT, [on line]. [Visited on January, 8th 2026]. Available on: https://www.fao.org/faostat/en/#data/QCL
KHORRAMI, Behzad, KHIAOSA-ARD, Ratchaneewan and ZEBELI, Qendrim, 2021. Models to predict the risk of subacute ruminal acidosis in dairy cows based on dietary and cow factors: A meta-analysis. Journal of Dairy Science. July 2021. Vol. 104, n° 7, pp. 7761‑7780. DOI 10.3168/jds.2020-19890.
KLEEN, J. L., HOOIJER, G. A., REHAGE, J. and NOORDHUIZEN, J. P. T. M., 2003. Subacute Ruminal Acidosis (SARA): a Review. Journal of Veterinary Medicine Series A. 2003. Vol. 50, n° 8, pp. 406‑414. DOI 10.1046/j.1439-0442.2003.00569.x.
LI, Wenli, GELSINGER, Sonia, EDWARDS, Andrea, RIEHLE, Christina and KOCH, Daniel, 2019. Transcriptome analysis of rumen epithelium and meta-transcriptome analysis of rumen epimural microbial community in young calves with feed induced acidosis. Scientific Reports. March 2019. Vol. 9, pp. 4744. DOI 10.1038/s41598-019-40375-2.
PLAIZIER, J. C., KRAUSE, D. O., GOZHO, G. N. and MCBRIDE, B. W., 2008. Subacute ruminal acidosis in dairy cows: The physiological causes, incidence and consequences. The Veterinary Journal. April 2008. Vol. 176, n° 1, pp. 21‑31. DOI 10.1016/j.tvjl.2007.12.016.
SAUVANT, D., REVERDIN, Stéphane et MESCHY, François, 2006. Le contrôle de l’acidose ruminale latente. INRA Productions Animales. 2006. Vol. 19, n° 2, pp. 69‑78.
