¿Qué es el nitrógeno?
El nitrógeno (N) es uno de los principales elementos que componen los organismos vivos, junto con el carbono, el oxígeno y el hidrógeno. En promedio, representa entre el 2,5 % y el 3,5 % de la materia orgánica seca de los animales. Los aminoácidos, que son los componentes básicos de las proteínas, son compuestos por un grupo amino (-NH2) que contiene nitrógeno y un grupo ácido carboxílico (-COOH). Por lo tanto, el nitrógeno es el tercer elemento más abundante en los aminoácidos, después del carbono (50-55 %) y el oxígeno (20-23 %). El nitrógeno es, por lo tanto, esencial para garantizar un metabolismo adecuado, la síntesis de proteínas y, por consiguiente, el crecimiento de los animales.
1. Necesidades proteicas, metabolismo en la acuicultura y emisiones de nitrógeno
25 a 40%
Estos son los requisitos medios de proteínas alimentarias de las especies acuícolas.
Las especies acuícolas suelen tener mayores necesidades proteicas que otros animales de granja, como las aves de corral (15-22 %) (Applegate y Angel, 2014). Estas mayores necesidades en aminoácidos se explican por la oxidación de los aminoácidos siendo la principal fuente de energía de los peces (Weber y Haman, 1996). Las necesidades proteicas de los peces varían según la especie y la dieta, oscilando entre el 25-35 % para las especies omnívoras y herbívoras, como la tilapia y la carpa, y el 35-40 % para las especies carnívoras, como los salmónidos, la lubina y la dorada.
Las proteínas ingeridas por los animales se descomponen rápidamente en aminoácidos en el tracto digestivo por la acción de diversas enzimas específicas: las pepsinas descomponen primero las proteínas en péptidos, y luego la tripsina y la quimotripsina descomponen los péptidos en aminoácidos (Engrola et al., 2009; Gamboa-Delgado et al., 2011). A continuación, estas células intestinales absorben los aminoácidos y los utilizan para sintetizar nuevas proteínas o para producir energía mediante desaminación (Bröer, 2008). El grupo amino se convierte en amoníaco (NH3), un producto de desecho metabólico que es tóxico para los animales si se acumula (Forster y Goldstein, 1969). Los organismos acuáticos pueden excretar rápidamente el NH3 al agua a través de sus branquias, evitando así su conversión y conservando energía en comparación con los animales uroteliales, como los mamíferos y las aves (Figura 1).
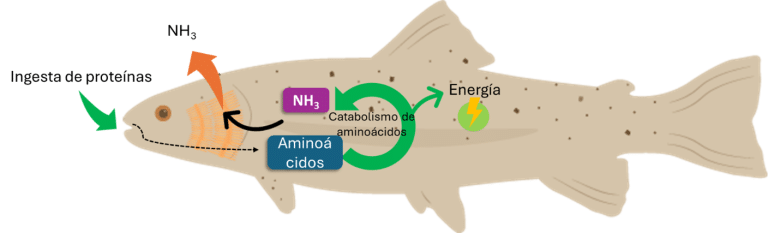
Figura 1: Metabolismo proteico y excreción de nitrógeno
(Evans et al., 2013; Weihrauch and O’Donnell, 2015)
2. El ciclo del nitrógeno y sus diversas formas en el agua.
Una vez liberado en el agua, el NH3 se diluye fácilmente. Dependiendo de los parámetros del agua, principalmente el pH y la temperatura, su forma dominante será el NH3 o el amonio (NH4+), una forma menos tóxica para los peces y los camarones, al capturar un ion H+ (Thurston y Russo, 1983). En el caso de un pH ácido, la forma dominante es el NH₄⁺, mientras que en el caso de un pH básico (>8,5), la forma más prevalente es el NH₃. La temperatura también influye en la ionización del NH₃, ya que las temperaturas más altas favorecen la forma NH₃ frente al NH₄⁺.
8.5
Es el pH que no debe superarse para limitar la formación de NH3.
Nitrificación
Es el proceso biológico que transforma el NH3 en NO2- y luego en NO3- mediante la acción de bacterias.
A continuación, el proceso biológico de nitrificación transforma el NH3 en nitrato (NO3–) bajo la acción de microorganismos. La nitrificación se divide en dos etapas distintas: nitrosación y nitración, cada una de ellas llevada a cabo por diferentes microorganismos. La nitrosación, llevada a cabo por bacterias de los géneros Nitrosomonas, Nitrosococcus y Nitrosospira, convierte el NH3 en nitrito (NO2–). La nitración, llevada a cabo en particular por los géneros Nitrobacter, Nitrococcus y Nitrospira, transforma el NO2– en nitrato (NO3–). La oxidación del NH3 y el NO2– proporciona a las bacterias la energía que necesitan para convertir el CO2 en materia orgánica (Figura 2).
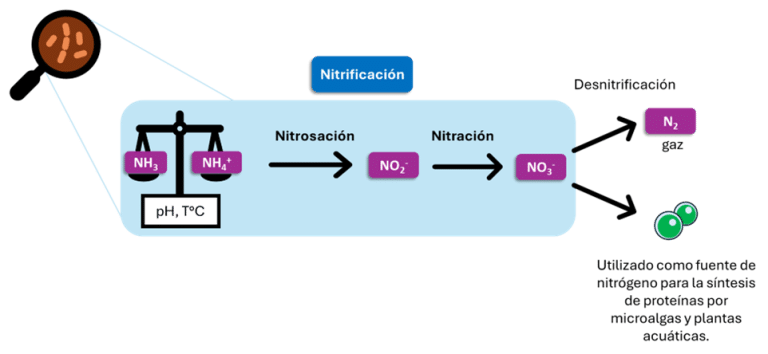
Figura 2: Ciclo del nitrógeno en el agua
(Robles-Porchas et al., 2020)
Para optimizar la nitrificación, es fundamental mantener un pH neutro, una buena oxigenación y un equilibrio redox en los estanques de peces y camarones (Molins-Legua et al., 2006). El NO3– producido por la nitrificación es absorbido y utilizado como fuente de nitrógeno por las plantas acuáticas y las algas, que reducen el NO3– a NH4+ para sintetizar aminoácidos y proteínas. Cualquier alteración del ciclo del nitrógeno puede afectar negativamente al rendimiento y a la supervivencia de los peces y camarones, ya que genera compuestos nitrogenados tóxicos, reduce la concentración de oxígeno (O2) y altera el pH del agua.
- En la trucha de lago (Salvelinus namaycush), la exposición a 198 µg/L de amoníaco durante 60 días reduce la eficiencia proteica por 7 % (Beamish y Tandler, 1990).
- Los alevines de trucha arcoíris (Oncorhynchus mykiss) expuestos a 13 mg/l de amoníaco durante 90 días después de la eclosión sufrieron una disminución de peso de 54 % y de su tasa de supervivencia de 70 % (Brinkman et al., 2009).
- En el camarón de patas blancas, la acumulación de nitritos y amoníaco procedentes de las heces y los restos de comida no consumida durante 33 días reduce las tasas de supervivencia en 2,5 veces y las tasas de crecimiento en un 20,5 % (Han et al., 2017).
- En el bagre de río (Ictalurus punctatus), la exposición a 3,71 mg/l durante 31 días reduce el crecimiento por 20 % (Colt et al., 1981).
3. Efectos nocivos del nitrógeno en el agua sobre los animales acuáticos
El nitrógeno liberado en el agua puede afectar directa o indirectamente a los animales acuáticos. Las diferentes formas de nitrógeno descritas anteriormente, incluyendo NH3, NH4+, NO2– y NO3–, tienen diferentes niveles de toxicidad para los peces y camarones. Si bien las concentraciones límite en el agua para los diversos compuestos de nitrógeno varían según la especie, el orden de toxicidad sigue siendo el mismo para todas las especies: el NH3 es el más tóxico, seguido por el NO2–, luego el NH4+ y finalmente el NO3– (Figura 3).
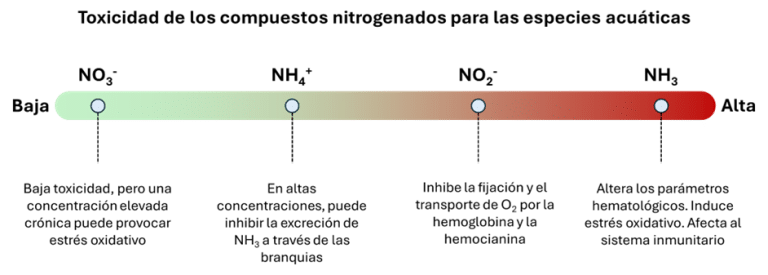
Figura 3: Toxicidad de los compuestos nitrogenados para las especies acuáticas
(Lin et al., 2023; Tomasso, 1994)
a. Toxicidad directa del nitrógeno
Dado que el NH3 es una molécula sin carga, puede difundirse fácilmente a través de las membranas biológicas, en particular las branquias (Klocke et al., 1972; Randall y Wright, 1987). Una vez en la sangre, altera muchos parámetros hematológicos, como el equilibrio ácido-base, la coagulación y el transporte de moléculas. En los peces, la acumulación de NH3 altera el sistema inmunitario, induce estrés oxidativo y causa daños en los tejidos de las branquias, el hígado, los riñones y los intestinos. En los crustáceos, el NH3 también induce estrés oxidativo y afecta al sistema inmunitario innato y a la muda (Bouwman et al., 2011; Chang et al., 2015; Cui et al., 2017; Hong et al., 2007; Rodríguez-Ramos et al., 2008; Romano y Zeng, 2013).
Efectos nocivos de los compuestos nitrogenados:
- Inmunosupresión
- Estrés oxidativo
- Neurotoxicidad
- Estrés branquial
El NO2– es menos tóxico que el NH3, pero su toxicidad sigue siendo muy alta. En los peces, el principal mecanismo de toxicidad del NO2– es la formación de metahemoglobina (MetHb) a través de la oxidación del hierro (Fe) en la hemoglobina. La MetHb ya no puede unirse y transportar O₂, lo que provoca hipoxia a pesar de que el agua esté oxigenado (Jensen, 2003). Se observa un fenómeno similar en los camarones: el NO2– oxida el cobre (Cu) de la hemocianina, lo que impide la unión del O₂. El NO2– también puede inducir estrés oxidativo y alterar el sistema inmunitario innato de los peces y los camarones. El NO2– también afecta a la biología y a la salud de las branquias (Svobodová et al., 2005), reduce la ingesta de alimentos en peces y camarones (Ribeiro-de-Campos et al., 2021; Roques et al., 2013) y afecta a su crecimiento (Ciji y Akhtar, 2020; Colt et al., 1981; Frances et al., 1998; Koo et al., 2005; Mallasen y Valenti, 2006; Siikavuopio y Sæther, 2006).
El NH4+ es mucho menos tóxico, y sus concentraciones en el agua deben ser muy altas para afectar a los animales acuáticos. En concentraciones elevadas, el NH4+ puede limitar la capacidad de las branquias para excretar NH3, lo que provoca la acumulación de NH3 en peces y camarones. El NH4+ también sustituye al potasio (K+) en los transportadores de iones, lo que afecta al gradiente electroquímico del sistema nervioso central (Cooper y Plum, 1987) y perjudica la función cerebral (Ip y Chew, 2010).
El NO3– tiene una toxicidad aguda baja, pero puede tener efectos crónicos significativos. El NO3– puede causar estrés oxidativo que, si es crónico, puede debilitar el sistema inmunitario, afectar a la reproducción y ralentizar el crecimiento. Su toxicidad depende de la concentración y el tiempo de exposición (Pierce et al., 1993; Scott y Crunkilton, 2000), así como de la salinidad (Dowden y Bennett, 1965).
b. Impactos indirectos de las emisiones de nitrógeno
Cuando la descarga de nitrógeno en el agua es excesiva, las bacterias nitrificantes pueden verse abrumadas por las altas concentraciones de NH3 y NO2–, lo que provoca su acumulación en el agua. El exceso de nitrógeno estimula el crecimiento y la proliferación de microalgas, lo que da lugar a la aparición de floraciones de algas. La alta concentración de microalgas reduce la penetración de la luz en la columna de agua, provocando su muerte. La descomposición de esta materia orgánica por las bacterias consume grandes cantidades de O₂, lo que reduce su concentración en el agua (Huo et al., 2013; Moss et al., 2013). Este fenómeno se denomina eutrofización (Figura 4).
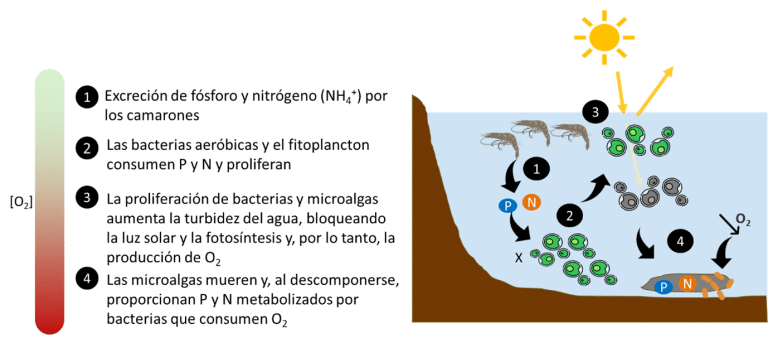
Figura 4: El proceso de eutrofización (Yang et al., 2008)
La eutrofización inicia un círculo vicioso, ya que la falta de O2 en el agua provoca la muerte de otros organismos acuáticos, lo que genera más materia orgánica y reduce aún más la concentración de O2 (Yang et al., 2008). Esto tiene un grave impacto en el crecimiento y la supervivencia de los peces y camarones, especialmente en los estanques, que son sistemas cerrados con poca renovación de agua. En particular, se ha observado que la proliferación de algas en los estanques de camarones en México, causada por un aporte excesivo de nutrientes, ha provocado una tasa de mortalidad del 79,5 % de las postlarvas, además de reducir el crecimiento corporal (Licea, 1999).
Además, la eutrofización puede provocar la proliferación de especies nocivas como las cianobacterias, que suelen tener un metabolismo anaeróbico, lo que significa que la disminución de la concentración de oxígeno en el agua favorece su proliferación (Codd, 2000). Se ha observado una disminución de la supervivencia de los camarones peneidos en China y Ecuador debido a la proliferación de microalgas que causan anoxia en los estanques (Alonso-Rodríguez y Páez-Osuna, 2003). En sistemas abiertos, como las jaulas marinas, los vertidos excesivos de nitrógeno pueden favorecer la proliferación de microalgas, algunas de las cuales producen toxinas (Anderson et al., 2002) o dañan las branquias de los peces con sus espículas (espinas calcáreas o silíceas), lo que puede provocar una mortalidad significativa en las piscifactorías afectadas (Burridge et al., 2010).
Los sistemas de recirculación acuícola (RAS), gracias a su capacidad para controlar los parámetros del agua, se ven menos afectados por estos problemas. Sin embargo, la descarga de nitrógeno sigue siendo un problema importante incluso para los sistemas más avanzados tecnológicamente. Los sistemas de filtración RAS son muy grandes y costosos de instalar. La reducción de los niveles de nitrógeno en el agua puede ayudar a evitar el sobredimensionamiento de los sistemas de filtración y, por lo tanto, limitar los costos. Además, la nitrificación consume la alcalinidad del agua, lo que requiere ajustes periódicos del pH (Timmons et al., 2018).
4. Las ventajas de reducir el aporte de nitrógeno en los sistemas acuícolas
Es esencial controlar los niveles de nitrógeno, tanto en instalaciones acuícolas cerradas (como tanques, estanques y sistemas de recirculación) para garantizar el rendimiento y el bienestar de los animales, como en sistemas abiertos (como jaulas marinas y canales) para minimizar su impacto medioambiental. Esto se puede lograr reduciendo las emisiones de nitrógeno al agua o mejorando la capacidad de las bacterias nitrificantes para convertir el nitrógeno. La reducción de las emisiones de nitrógeno implica optimizar la distribución del alimento para evitar la sobrealimentación y ajustar la formulación del alimento para limitar la ingestión de nitrógeno. Modulando con precisión los niveles de proteínas en el pienso en relación con otros nutrientes, se puede reducir el catabolismo de las proteínas y las emisiones de amoníaco (NH3) al agua.
Esto también implica elegir otras materias primas, como los fosfatos inorgánicos para piensos. Es fundamental elegir productos que limiten las emisiones de fósforo (P) y nitrógeno (N) para evitar su acumulación en el agua y, por lo tanto, prevenir la eutrofización. Para este fin, el fosfato monosódico (MSP) es la mejor opción, ya que proporciona P altamente digerible para los peces y camarones, al tiempo que reduce las emisiones de N al agua en comparación con el fosfato monoamónico (MAP) (Morales et al., 2018). Aunque el fosfato MAP también proporciona P altamente digestible, también proporciona un exceso de NH3 que no es utilizado por los organismos acuáticos de la misma manera que lo hacen los rumiantes.
Por lo tanto, aunque el MAP es un fosfato eficaz para la acuicultura, aumenta las emisiones de nitrógeno al agua (Figura 5). Por lo tanto, para proporcionar una fuente eficaz de P y reducir al mismo tiempo las emisiones de P y N, que afectan a la salud de los peces y al medio ambiente, es preferible optar por el MSP.
4.2kg
Es la reducción del N disuelto excretado en el agua por tonelada de pescado producido utilizando MSP en comparación con MAP (Morales et al., 2018).
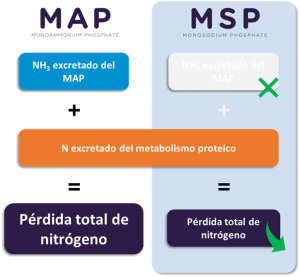
Figura 5: Reducción de las emisiones de N con el MSP
Conclusión
El nitrógeno es un elemento esencial en la acuicultura, pero su metabolismo puede generar residuos tóxicos como el NH3 cuando se acumula en el agua. Por lo tanto, es necesario realizar ajustes en la dieta para reducir las emisiones de N y crear condiciones óptimas para las bacterias nitrificantes, con el fin de minimizar los efectos nocivos del N y garantizar la salud de las especies acuícolas. En términos de alimentación e ingesta de P inorgánico, el MSP es la fuente más adecuada para garantizar la sostenibilidad de las granjas acuícolas.
Bibliografía
Alonso-Rodrı́guez, R., Páez-Osuna, F., 2003. Nutrients, phytoplankton and harmful algal blooms in shrimp ponds: a review with special reference to the situation in the Gulf of California. Aquaculture 219, 317–336. https://doi.org/10.1016/S0044-8486(02)00509-4
Anderson, D.M., Glibert, P.M., Burkholder, J.M., 2002. Harmful algal blooms and eutrophication: Nutrient sources, composition, and consequences. Estuaries 25, 704–726. https://doi.org/10.1007/BF02804901
Applegate, T.J., Angel, R., 2014. Nutrient requirements of poultry publication: History and need for an update. J. Appl. Poult. Res. 23, 567–575. https://doi.org/10.3382/japr.2014-00980
Beamish, F.W.H., Tandler, A., 1990. Ambient ammonia, diet and growth in lake trout. Aquat. Toxicol. 17, 155–166. https://doi.org/10.1016/0166-445X(90)90028-N
Bouwman, A.F., Pawłowski, M., Liu, C., Beusen, A.H.W., Shumway, S.E., Glibert, P.M., Overbeek, C.C., 2011. Global Hindcasts and Future Projections of Coastal Nitrogen and Phosphorus Loads Due to Shellfish and Seaweed Aquaculture. Rev. Fish. Sci. 19, 331–357. https://doi.org/10.1080/10641262.2011.603849
Brinkman, S.F., Woodling, J.D., Vajda, A.M., Norris, D.O., 2009. Chronic Toxicity of Ammonia to Early Life Stage Rainbow Trout. Trans. Am. Fish. Soc. 138, 433–440. https://doi.org/10.1577/T07-224.1
Bröer, S., 2008. Amino Acid Transport Across Mammalian Intestinal and Renal Epithelia. Physiol. Rev. 88, 249–286. https://doi.org/10.1152/physrev.00018.2006
Burridge, L., Weis, J.S., Cabello, F., Pizarro, J., Bostick, K., 2010. Chemical use in salmon aquaculture: A review of current practices and possible environmental effects. Aquaculture 306, 7–23. https://doi.org/10.1016/j.aquaculture.2010.05.020
Chang, Z.-W., Chiang, P.-C., Cheng, W., Chang, C.-C., 2015. Impact of ammonia exposure on coagulation in white shrimp, Litopenaeus vannamei. Ecotoxicol. Environ. Saf. 118, 98–102. https://doi.org/10.1016/j.ecoenv.2015.04.019
Ciji, A., Akhtar, M.S., 2020. Nitrite implications and its management strategies in aquaculture: a review. Rev. Aquac. 12, 878–908. https://doi.org/10.1111/raq.12354
Codd, G.A., 2000. Cyanobacterial toxins, the perception of water quality, and the prioritisation of eutrophication control. Ecol. Eng. 16, 51–60. https://doi.org/10.1016/S0925-8574(00)00089-6
Colt, J., Ludwig, R., Tchobanoglous, G., Cech, J.J., 1981. The effects of nitrite on the short-term growth and survival of channel catfish, Ictalurus punctatus. Aquaculture 24, 111–122. https://doi.org/10.1016/0044-8486(81)90048-X
Cooper, A.J., Plum, F., 1987. Biochemistry and physiology of brain ammonia. Physiol. Rev. 67, 440–519. https://doi.org/10.1152/physrev.1987.67.2.440
Cui, Y., Ren, X., Li, J., Zhai, Q., Feng, Y., Xu, Y., Ma, L., 2017. Effects of ammonia-N stress on metabolic and immune function via the neuroendocrine system in Litopenaeus vannamei. Fish Shellfish Immunol. 64, 270–275. https://doi.org/10.1016/j.fsi.2017.03.028
Dowden, B.F., Bennett, H.J., 1965. Toxicity of Selected Chemicals to Certain Animals. J. Water Pollut. Control Fed. 37, 1308–1316.
Engrola, S., Mai, M., Dinis, M.T., Conceição, L.E.C., 2009. Co-feeding of inert diet from mouth opening does not impair protein utilization by Senegalese sole (Solea senegalensis) larvae. Aquaculture 287, 185–190. https://doi.org/10.1016/j.aquaculture.2008.10.036
Evans, D.H., Claiborne, J.B., Currie, S., 2013. The Physiology of Fishes, Fourth Edition. CRC Press.
Forster, R.P., Goldstein, L., 1969. 5 Formation of Excretory Products, in: Hoar, W.S., Randall, D.J. (Eds.), Fish Physiology, Excretion, Ionic Regulation, and Metabolism. Academic Press, pp. 313–350. https://doi.org/10.1016/S1546-5098(08)60086-2
Frances, J., Allan, G.L., Nowak, B.F., 1998. The effects of nitrite on the short-term growth of silver perch (Bidyanus bidyanus). Aquaculture 163, 63–72. https://doi.org/10.1016/S0044-8486(98)00219-1
Gamboa-Delgado, J., Peña-Rodríguez, A., Ricque-Marie, D., Cruz-Suárez, L.E., 2011. Assessment of Nutrient Allocation and Metabolic Turnover Rate in Pacific White Shrimp Litopenaeus vannamei Co-Fed Live Macroalgae Ulva clathrata and Inert Feed: Dual Stable Isotope Analysis. J. Shellfish Res. 30, 969–978. https://doi.org/10.2983/035.030.0340
Han, S., Wang, B., Wang, M., Liu, Q., Zhao, W., Wang, L., 2017. Effects of ammonia and nitrite accumulation on the survival and growth performance of white shrimp Litopenaeus vannamei. Invertebr. Surviv. J. 14, 221–232. https://doi.org/10.25431/1824-307X/isj.v14i1.221-232
Hong, M., Chen, L., Sun, X., Gu, S., Zhang, L., Chen, Y., 2007. Metabolic and immune responses in Chinese mitten-handed crab (Eriocheir sinensis) juveniles exposed to elevated ambient ammonia. Comp. Biochem. Physiol. Part C Toxicol. Pharmacol. 145, 363–369. https://doi.org/10.1016/j.cbpc.2007.01.003
Huo, S., Ma, C., Xi, B., Su, J., Zan, F., Ji, D., He, Z., 2013. Establishing eutrophication assessment standards for four lake regions, China. J. Environ. Sci. 25, 2014–2022. https://doi.org/10.1016/S1001-0742(12)60250-2
Ip, A.Y.K., Chew, S.F., 2010. Ammonia Production, Excretion, Toxicity, and Defense in Fish: A Review. Front. Physiol. 1. https://doi.org/10.3389/fphys.2010.00134
Jensen, F.B., 2003. Nitrite disrupts multiple physiological functions in aquatic animals. Comp. Biochem. Physiol. A. Mol. Integr. Physiol. 135, 9–24. https://doi.org/10.1016/s1095-6433(02)00323-9
Kaushik, S.J., 1998. Whole body amino acid composition of European seabass (Dicentrarchus labrax), gilthead seabream (Sparus aurata) and turbot (Psetta maxima) with an estimation of their IAA requirement profiles. Aquat. Living Resour. 11, 355–358. https://doi.org/10.1016/S0990-7440(98)80007-7
Klocke, R., Andersson, K., Rotman, H., Forster, R., 1972. Permeability of human erythrocytes to ammonia and weak acids. Am. J. Physiol.-Leg. Content 222, 1004–1013. https://doi.org/10.1152/ajplegacy.1972.222.4.1004
Koo, J.-G., Kim, S.-G., Jee, J.-H., Kim, J.-M., Bai, S.C., Kang, J.-C., 2005. Effects of ammonia and nitrite on survival, growth and moulting in juvenile tiger crab, Orithyia sinica (Linnaeus). Aquac. Res. 36, 79–85. https://doi.org/10.1111/j.1365-2109.2004.01187.x
Licea, S., 1999. Proliferaciones de microalgas nocivas en los estanques para el cultivo semi-intensivo de camarón en México. Rev. Latinoam. Microbiol. 38, 123.
Lin, W., Luo, H., Wu, J., Hung, T.-C., Cao, B., Liu, X., Yang, J., Yang, P., 2023. A Review of the Emerging Risks of Acute Ammonia Nitrogen Toxicity to Aquatic Decapod Crustaceans. Water 15, 27. https://doi.org/10.3390/w15010027
Mallasen, M., Valenti, W.C., 2006. Effect of nitrite on larval development of giant river prawn Macrobrachium rosenbergii. Aquaculture 261, 1292–1298. https://doi.org/10.1016/j.aquaculture.2006.07.048
Molins-Legua, C., Meseguer-Lloret, S., Moliner-Martinez, Y., Campíns-Falcó, P., 2006. A guide for selecting the most appropriate method for ammonium determination in water analysis. TrAC Trends Anal. Chem. 25, 282–290. https://doi.org/10.1016/j.trac.2005.12.002
Morales, G.A., Azcuy, R.L., Casaretto, M.E., Márquez, L., Hernández, A.J., Gómez, F., Koppe, W., Mereu, A., 2018. Effect of different inorganic phosphorus sources on growth performance, digestibility, retention efficiency and discharge of nutrients in rainbow trout (Oncorhynchus mykiss). Aquaculture 495, 568–574. https://doi.org/10.1016/j.aquaculture.2018.06.036
Moss, B., Jeppesen, E., Søndergaard, M., Lauridsen, T.L., Liu, Z., 2013. Nitrogen, macrophytes, shallow lakes and nutrient limitation: resolution of a current controversy? Hydrobiologia 710, 3–21. https://doi.org/10.1007/s10750-012-1033-0
Nutrient Requirements of Fish and Shrimp, 2011. . National Academies Press, Washington, D.C. https://doi.org/10.17226/13039
Pierce, R.H., Weeks, J.M., Prappas, J.M., 1993. Nitrate Toxicity to Five Species of Marine Fish. J. World Aquac. Soc. 24, 105–107. https://doi.org/10.1111/j.1749-7345.1993.tb00156.x
Pinho, S.M., Emerenciano, M.G.C., 2021. Sensorial attributes and growth performance of whiteleg shrimp (Litopenaeus vannamei) cultured in biofloc technology with varying water salinity and dietary protein content. Aquaculture 540, 736727. https://doi.org/10.1016/j.aquaculture.2021.736727
Randall, D.J., Wright, P.A., 1987. Ammonia distribution and excretion in fish. Fish Physiol. Biochem. 3, 107–120. https://doi.org/10.1007/BF02180412
Ribeiro-de-Campos, B., Ortiz-Kracizy, R., Furtado, P.S., Volkweis-Zadinelo, I., Cupertino-Ballester, E.L., Ribeiro-de-Campos, B., Ortiz-Kracizy, R., Furtado, P.S., Volkweis-Zadinelo, I., Cupertino-Ballester, E.L., 2021. Effects of ammonia and nitrite on food consumption of the Amazon River prawn Macrobrachium amazonicum (Heller, 1862) postlarvae. Lat. Am. J. Aquat. Res. 49, 684–688. https://doi.org/10.3856/vol49-issue4-fulltext-2583
Robles-Porchas, G.R., Gollas-Galván, T., Martínez-Porchas, M., Martínez-Cordova, L.R., Miranda-Baeza, A., Vargas-Albores, F., 2020. The nitrification process for nitrogen removal in biofloc system aquaculture. Rev. Aquac. 12, 2228–2249. https://doi.org/10.1111/raq.12431
Rodríguez-Ramos, T., Espinosa, G., Hernández-López, J., Gollas-Galván, T., Marrero, J., Borrell, Y., Alonso, M.E., Bécquer, U., Alonso, M., 2008. Effects of Echerichia coli lipopolysaccharides and dissolved ammonia on immune response in southern white shrimp Litopenaeus schmitti. Aquaculture 274, 118–125. https://doi.org/10.1016/j.aquaculture.2007.10.049
Romano, N., Zeng, C., 2013. Toxic Effects of Ammonia, Nitrite, and Nitrate to Decapod Crustaceans: A Review on Factors Influencing their Toxicity, Physiological Consequences, and Coping Mechanisms. Rev. Fish. Sci. 21, 1–21. https://doi.org/10.1080/10641262.2012.753404
Roques, J., Schram, E., Spanings, T., 2013. The impact of elevated water nitrite concentration on physiology, growth and feed intake of African catfish Clarias gariepinus (Burchell 1822) – Roques – 2015 – Aquaculture Research – Wiley Online Library [WWW Document]. URL https://onlinelibrary.wiley.com/doi/abs/10.1111/are.12292 (accessed 10.29.25).
Scott, G., Crunkilton, R.L., 2000. Acute and chronic toxicity of nitrate to fathead minnows (Pimephales promelas), ceriodaphnia dubia, and Daphnia magna. Environ. Toxicol. Chem. 19, 2918–2922. https://doi.org/10.1002/etc.5620191211
Siikavuopio, S.I., Sæther, B.-S., 2006. Effects of chronic nitrite exposure on growth in juvenile Atlantic cod, Gadus morhua. Aquaculture 255, 351–356. https://doi.org/10.1016/j.aquaculture.2005.11.058
Svobodová, Z., Máchová, J., Poleszczuk, G., Hůda, J., Hamáčková, J., Kroupová, H., 2005. Nitrite Poisoning of Fish in Aquaculture Facilities with Water-recirculating Systems. Acta Vet. Brno 74, 129–137. https://doi.org/10.2754/avb200574010129
Thurston, R.V., Russo, R.C., 1983. Acute Toxicity of Ammonia to Rainbow Trout. Trans. Am. Fish. Soc. 112, 696–704. https://doi.org/10.1577/1548-8659(1983)112<696:ATOATR>2.0.CO;2
Timmons, M., Guerdat, T., Vinci, B., 2018. Recirculating Aquaculture, 4th edition.
Tomasso, J.R., 1994. Toxicity of nitrogenous wastes to aquaculture animals. Rev. Fish. Sci. 2, 291–314. https://doi.org/10.1080/10641269409388560
Weber, J.-M., Haman, F., 1996. Pathways for metabolic fuels and oxygen in high performance fish. Comp. Biochem. Physiol. A Physiol. 113, 33–38. https://doi.org/10.1016/0300-9629(95)02063-2
Weerd, J.H.V., 1995. Nutrition and growth in Clarias species – a review. Aquat. Living Resour. 8, 395–401. https://doi.org/10.1051/alr:1995046
Weihrauch, D., O’Donnell, M.J., 2015. Links between Osmoregulation and Nitrogen-Excretion in Insects and Crustaceans. Integr. Comp. Biol. 55, 816–829. https://doi.org/10.1093/icb/icv013
Yang, X., Wu, X., Hao, H., He, Z., 2008. Mechanisms and assessment of water eutrophication. J. Zhejiang Univ. Sci. B 9, 197–209. https://doi.org/10.1631/jzus.B0710626
