Introdução
Os ruminantes diferem de outros animais devido ao seu sistema digestivo: possuem um rúmen. O rúmen é o principal ator da digestão nos ruminantes e abriga os microrganismos responsáveis pela fermentação biológica dos alimentos. Assim, alimentar um ruminante é alimentar seu microbiota ruminal. Originalmente, os ruminantes são adaptados a digerir principalmente forragens, mas a evolução dos sistemas de produção transformou sua dieta. A produção mundial de leite aumentou em mais de 142 milhões de toneladas em dez anos (+ 21,7%; FAO, 2024). Para aumentar a produção de leite ou o desempenho de engorda, os produtores utilizam dietas mais intensivas que, se não forem bem manejadas, alteram o ambiente ruminal e levam a uma acidose ruminal subclínica (Sub-Acute Ruminal Acidosis ou SARA, em inglês). A SARA é um problema muito comum em ruminantes, pois entre 19% e 26% das vacas de rebanhos leiteiros intensivos apresentam SARA (Kleen et al. 2013). A presença de SARA está associada a perturbações significativas na saúde e no desempenho animal, incluindo uma redução de 10% na digestibilidade da fibra (Orne Conseil Élevage, 2016), e uma redução média de 2,7 kg de leite produzido por vaca por dia (Enemark, 2008). Este dossiê técnico detalhará as consequências e estratégias de gestão da SARA.
O que é a acidose ruminal subclínica?
A acidose ruminal subclínica (SARA) é um dos principais problemas nutricionais nas vacas leiteiras. Este distúrbio metabólico provoca uma alteração na fermentação ruminal, causada por uma transição alimentar inadequada e/ou por uma composição inadequada da dieta. A SARA resulta de um desequilíbrio da microbiota ruminal, causado por uma dieta rica em carboidratos fermentáveis e/ou pobre em proteínas, e representa uma ameaça constante para os ruminantes de alto nível produtivo.
O pH ótimo do rúmen para vacas leiteiras de alta produção situa-se entre 6 e 6,5, o que permite um bom equilíbrio da microbiota ruminal. No entanto, devido às estratégias alimentares intensivas, observam-se flutuações diárias do pH ruminal, o que induz de forma irreversível, degradação das papilas ruminais e diminuição da capacidade de absorção de nutrientes (Figura 1). Consequentemente, essas flutuações diárias do pH ruminal prejudicam a saúde e o desempenho zootécnico dos animais.
El pH óptimo del rumen para las vacas lecheras de alta producción se sitúa entre 6 y 6.5, lo que permite un equilibrio adecuado de la microbiota ruminal. Sin embargo, debido a las estrategias alimentarias intensivas, se observan fluctuaciones diarias del pH ruminal, lo que induce de manera irreversible una degradación de las papilas ruminales y una disminución de la capacidad de absorción de nutrientes (Figura 1). Como consecuencia, estas fluctuaciones diarias del pH ruminal deterioran la salud y el rendimiento zootécnico de los animales.
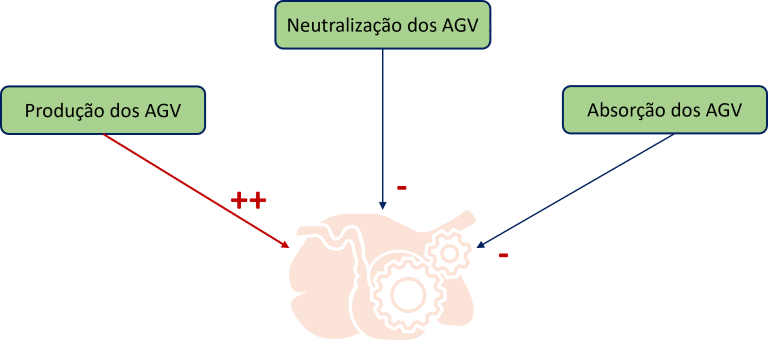
Figura 1: Origem da acidose subclínica.
A acidose ruminal pode ser definida como uma queda do pH ruminal quando a produção de ácidos, especialmente ácidos graxos voláteis (AGV), supera a capacidade de neutralização e de absorção. Existem duas formas de acidose ruminal: a acidose aguda e a acidose subclínica ou subaguda (Sauvant, Reverdin e Meschy, 2006). É esta última que será desenvolvida a seguir.
A SARA é a consequência de um desequilíbrio energia/proteína na dieta
Os micro-organismos ruminais são muito sensíveis às flutuações diárias do pH. Para otimizar o desempenho, por meio de maior densidade energética da dieta, as vacas permanecem constantemente no limite da SARA. De acordo com Plaizier et al., (2008), a SARA pode ser descrita por um pH ruminal médio inferior a 5,6, por mais de 3,5 horas por dia. De fato, quando o pH ruminal desce abaixo de 6, a atividade celulolítica diminui, enquanto a atividade amilolítica aumenta (Figura 2). O rúmen não funciona corretamente: as fermentações ruminais são reduzidas. Como as bactérias celulolíticas permitem digerir a fibra da dieta, a digestão se torna incompleta. É um círculo vicioso, pois, se esse desequilíbrio não for corrigido rapidamente, as atividades enzimáticas dos lactobacilos (tolerantes a pH baixo) continuam a aumentar, o que induz aumento da produção de ácido lático e acentuada diminuição do pH ruminal. As fermentações no rúmen continuam a desacelerar até parar por completo, e as consequências (técnico-econômicas) podem ser consideráveis.
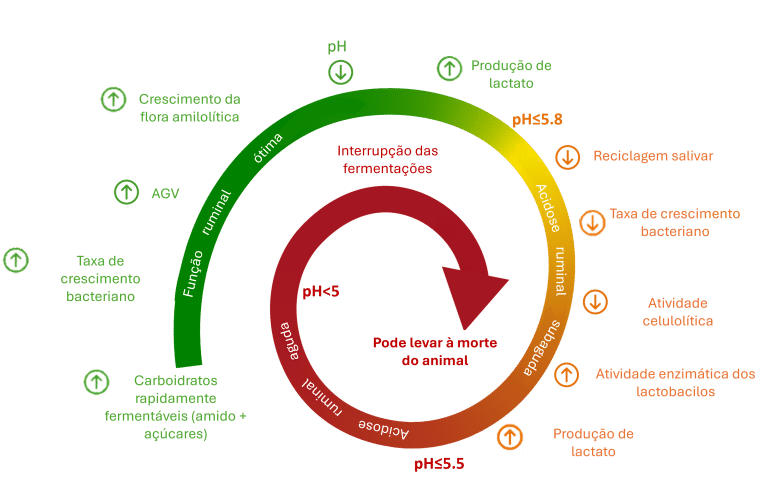
Figura 2: Círculo vicioso da acidose. Adaptado de Hernandez et al., 2014.
Transição alimentar: um período de alto risco para vacas
As variações naturais nos silos de milho ou de capim, ao longo do tempo, colocam à prova a estabilidade da dieta. De fato, a silagem de milho continua a evoluir algumas semanas após a ensilagem. A silagem de milho proveniente de uma única colheita pode apresentar variações semanais em seus valores nutricionais (por exemplo: teor de açúcares, digestibilidade do amido, teor de matéria seca, …). No entanto, com os baixos rendimentos obtidos dos últimos anos, devido à seca, torna-se cada vez mais difícil deixar fermentar a silagem de milho por 1 a 3 meses antes de começá-la. Por isso, as vacas são alimentadas com forragens frescas, o que pode provocar distúrbios digestivos. Em comparação com as forragens conservadas, as forragens frescas não têm tempo suficiente para fermentar, o que aumenta o risco de SARA no animal. Como resultado, a estabilidade da microbiota ruminal é afetada. De fato, a silagem fresca é rica em açúcares rapidamente fermentáveis. Uma vez no rúmen, esses açúcares provocam fermentações rápidas e desequilibradas. A flora amilolítica é superestimulada, o que leva à produção de grandes quantidades de AGV, notadamente propionato e butirato. Como explicado anteriormente, essa elevada produção de AGV supera a taxa de absorção pela parede ruminal e a capacidade de neutralização pela saliva, o que aumenta o risco de SARA.
Dificuldades semelhantes ocorrem com o capim da primavera e do outono. De fato, o capim novo é muito rico em carboidratos rapidamente fermentáveis (amido e açúcares), rico em nitrogênio e pobre em fibras. Muito palatável para os animais, é consumido rapidamente, o que diminui a salivação e aumenta o risco de SARA. Devido a seu alto teor de bicarbonato de sódio (12,5 g/L; Erdman, (1988)), a saliva constitui um tampão natural para o pH ruminal. Assim, uma produção reduzida de saliva implica menos efeito tampão no rúmen.
Níveis elevados de amido e a fonte do amido aumentam o risco de SARA
A composição da dieta é um fator-chave na manejo da SARA. Por exemplo, o teor de amido, assim como sua origem, podem aumentar o risco de SARA. Elmhadi et al. (2022) afirmam que um teor de amido entre 50% e 65% pode induzir SARA. Khorrami et al. (2021) confirmam que o tempo com pH ruminal baixo (< 6) aumenta com o teor de amido na dieta. Eles também constataram que o tipo de amido utilizado pode influenciar o risco de SARA. O amido de milho é mais acidogênico do que a cevada e o trigo, quando fornecido em grandes quantidades (> 20% da matéria seca total; Khorrami et al., 2021).
Como detectar a SARA?
As consequências da SARA podem ser numerosas e variar de um animal para outro. Podem se manifestar como uma ou mais observações visuais listadas na Figura 3.
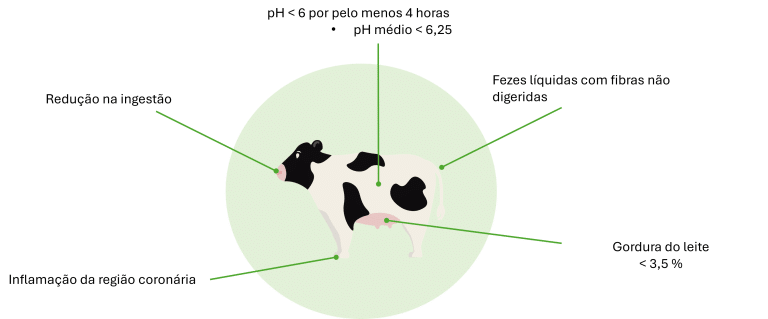
Figura 3: Como reconhecer a SARA nos animais?
Ao reduzir a matéria seca ingerida (MSI; -2,3 kg/dia em média com a SARA) e afetar a atividade do rúmen, a SARA conduz a uma diminuição na produção de leite, que pode situar-se entre 1,8 kg/dia e 3,3 kg/dia segundo Chiquette et al. (2015). Além dessa perda de produção, a menor atividade das bactérias celulolíticas afeta o teor de gordura do leite devido à menor produção de acetato, um AGV precursor de gordura láctea. Chiquette et al. (2015) observaram uma diminuição de 0,18% no percentual de gordura do leite durante um desafio de SARA. Em animais jovens, a SARA também está associada a redução da MSI e do ganho de peso médio em bezerros antes do desmame (Wenli Li et al., 2019). Além disso, a SARA pode afetar indiretamente o desempenho reprodutivo. De fato, menor eficiência alimentar pode resultar em um escore de condição corporal insuficiente, o que afeta a reprodução. Como demonstrado por Seesupa et al. (2017), a SARA também pode alterar o sistema hormonal, levando a menor fertilidade. Considerando tudo isso, a SARA representa um custo para o produtor, que pode perder entre 1,12 e 1,2€/vaca/dia (Plaizier et al., 2008).
Como limitar o risco de SARA?
Para reduzir o risco de SARA, é importante respeitar os princípios fundamentais da nutrição dos ruminantes:
- Realizar transições alimentares progressivas
- Fornecer água suficiente
- Garantir consumo regular de alimentos ao longo do dia
- Analisar a forragem para obter dieta equilibrada em energia e proteína
O perfil nutricional, em termos de amido e fibras, também é muito importante. Em particular, o teor e a qualidade da fibra são essenciais para gerir o risco de SARA. Como mencionado por Khorrami et al. (2021), os casos de SARA aumentam quando o teor de amido ultrapassa 20% e a peNDF > 8 (peNDF é a fibra detergente neutra fisicamente eficaz, isto é, uma tamanho de partícula superior a 8 mm) é inferior a 14%. No entanto, a peNDF não deve ser muito elevada para não limitar a MSI.
O uso sistemático ou direcionado, durante períodos de risco, de soluções tampão representa uma estratégia-chave para apoiar os animais e manter uma atividade ruminal ótima no contexto do manejo da SARA. Na Phosphea, estamos empenhados em contribuir para limitar o risco de SARA, oferecendo nossa solução tampão natural: CALSEA Powder.
Como o CALSEA Powder pode contribuir para o manejo da SARA?
CALSEA Powder é uma solução natural baseada 100% em algas marinhas calcárias (Lithothamnium calcareum). A estrutura porosa dessas algas, combinada com sua estrutura cristalina única, permite uma forte solubilização e uma liberação rápida de íons de cálcio e de carbonato no rúmen, o que permite uma melhor manutenção do pH ruminal.
As vacas que recebem o tratamento com bicarbonato de sódio (SBC; 200 g/vaca/dia) apresentam pH ruminal médio mais baixo do que aquelas com o tratamento CALSEA (100 g/vaca/dia; Figura 4). O pH ruminal mínimo obtido com o tratamento SBC é de 5,45, significativamente inferior ao obtido com CALSEA (Figura 4). Além disso, com CALSEA, o percentual de animais com pH ruminal < 5,5 é significativamente inferior ao do SBC (Figura 4). Um pH < 6, por pelo menos 4 horas, representa risco de acidose e, quando o pH é <5,5, esse risco é elevado. Segundo os resultados, a capacidade tamponante do CALSEA é superior à do SBC.
CALSEA Powder atua como solução tampão promovendo a estabilidade do pH ruminal, com efeitos positivos sobre as populações microbianas ruminais e um menor risco de SARA. A Figura 5 mostra a abundância relativa de algumas bactérias indicadoras do estado de SARA com diferentes soluções tampão.
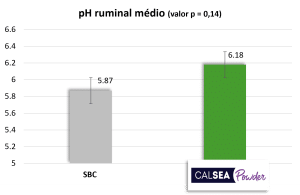
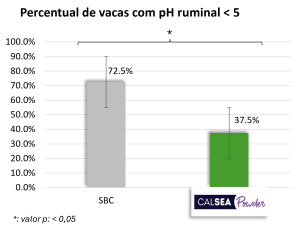
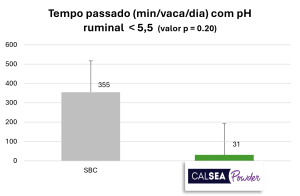
Figura 4: Ação do CALSEA Powder sobre o pH ruminal, em comparação ao bicarbonato de sódio (ensaio in vivo; n=40).
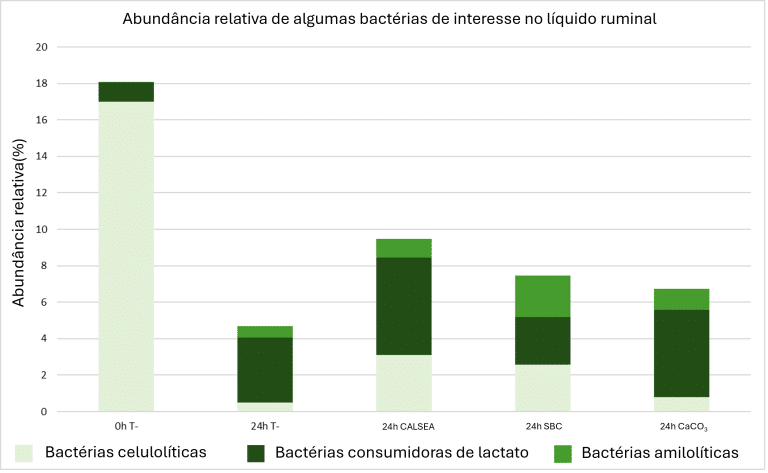
Figura 5: Monitoramento in vitro das populações bacterianas ruminais em caso de acidose ruminal subclínica (T-: Controle com SARA).
0h T- representa o controle negativo sem tampão no tempo 0. Nesse estágio, o efeito acidogênico da dieta não é visível e a situação é considerada normal. Após 24 horas de fermentação sem tampão (24h T-), a SARA se instala e afeta negativamente as bactérias celulolíticas, cuja população diminui drasticamente. Em comparação com o controle negativo (T-24h), CALSEA (100 g/vaca/dia) e o SBC (200 g/vaca/dia) parecem estimular a atividade celulolítica (Fibrobacter). As bactérias consumidoras de lactato (Megasphaera) são mais presentes com CALSEA e CaCO3 do que com SBC. Esta última bactéria protege contra a SARA porque consome ácido lático. Este ensaio mostra que CALSEA favorece a atividade bacteriana celulolítica em condições acidogênicas, contribuindo para manter uma eficiência ruminal ótima.
Products tailored to your livestock's need
Bibliografía
CHIQUETTE, J., LAGROST, J., GIRARD, C.L., TALBOT, G., LI, S., PLAIZIER, J.C. and HINDRICHSEN, I.K., 2015. Efficacy of the direct-fed microbial Enterococcus faecium alone or in combination with Saccharomyces cerevisiae or Lactococcus lactis during induced subacute ruminal acidosis. Journal of Dairy Science. January 2015. Vol. 98, n° 1, pp. 190‑203. DOI 10.3168/jds.2014-8219.
ELMHADI, Mawda E., ALI, Darien K., KHOGALI, Mawahib K. and WANG, Hongrong, 2022. Subacute ruminal acidosis in dairy herds: Microbiological and nutritional causes, consequences, and prevention strategies. Animal Nutrition. September 2022. Vol. 10, pp. 148‑155. DOI 10.1016/j.aninu.2021.12.008.
ENEMARK, Jörg M. D., 2008. The monitoring, prevention and treatment of sub-acute ruminal acidosis (SARA): A review. The Veterinary Journal. April 2008. Vol. 176, n° 1, pp. 32‑43. DOI 10.1016/j.tvjl.2007.12.021.
ERDMAN, Richard A., 1988. Dietary Buffering Requirements of the Lactating Dairy Cow: A Review1. Journal of Dairy Science. December 1988. Vol. 71, n° 12, pp. 3246‑3266. DOI 10.3168/jds.S0022-0302(88)79930-0.
FAOSTAT, [on line]. [Visited on January, 8th 2026]. Available on: https://www.fao.org/faostat/en/#data/QCL
KHORRAMI, Behzad, KHIAOSA-ARD, Ratchaneewan and ZEBELI, Qendrim, 2021. Models to predict the risk of subacute ruminal acidosis in dairy cows based on dietary and cow factors: A meta-analysis. Journal of Dairy Science. July 2021. Vol. 104, n° 7, pp. 7761‑7780. DOI 10.3168/jds.2020-19890.
KLEEN, J. L., HOOIJER, G. A., REHAGE, J. and NOORDHUIZEN, J. P. T. M., 2003. Subacute Ruminal Acidosis (SARA): a Review. Journal of Veterinary Medicine Series A. 2003. Vol. 50, n° 8, pp. 406‑414. DOI 10.1046/j.1439-0442.2003.00569.x.
LI, Wenli, GELSINGER, Sonia, EDWARDS, Andrea, RIEHLE, Christina and KOCH, Daniel, 2019. Transcriptome analysis of rumen epithelium and meta-transcriptome analysis of rumen epimural microbial community in young calves with feed induced acidosis. Scientific Reports. March 2019. Vol. 9, pp. 4744. DOI 10.1038/s41598-019-40375-2.
PLAIZIER, J. C., KRAUSE, D. O., GOZHO, G. N. and MCBRIDE, B. W., 2008. Subacute ruminal acidosis in dairy cows: The physiological causes, incidence and consequences. The Veterinary Journal. April 2008. Vol. 176, n° 1, pp. 21‑31. DOI 10.1016/j.tvjl.2007.12.016.
SAUVANT, D., REVERDIN, Stéphane et MESCHY, François, 2006. Le contrôle de l’acidose ruminale latente. INRA Productions Animales. 2006. Vol. 19, n° 2, pp. 69‑78.
