Introduction
Les ruminants diffèrent des autres animaux de par leur système digestif : ils possèdent un rumen. Le rumen est le principal acteur de la digestion chez le ruminant, il abrite les microorganismes responsables de la fermentation biologique des aliments. Ainsi, nourrir un ruminant, c’est nourrir son microbiote ruminal. À l’origine, les ruminants sont adaptés à digérer principalement les fourrages, mais l’évolution des systèmes de production a transformé leur régime alimentaire. La production mondiale de lait a augmenté de plus de 142 millions de tonnes en dix ans (+ 21,7 % ; FAO, 2024). Pour augmenter la production de lait ou les performances d’engraissement, les éleveurs utilisent des régimes plus intensifs qui, s’ils ne sont pas bien gérés, perturbent l’environnement ruminal et conduisent à une acidose ruminale subclinique (Sub-Acute Ruminal Acidosis ou SARA, en anglais). La SARA est un problème très courant chez les ruminants, car 19 % à 26 % des vaches des troupeaux laitiers intensifs sont affectées par la SARA (Kleen et al. 2013). La présence de SARA est associée à des perturbations importantes de la santé et des performances animales, notamment une baisse de 10 % de la digestibilité des fibres (Orne Conseil Elevage, 2016), et une réduction moyenne de 2,7 kg de lait produit par vache et par jour (Enemark, 2008). Ce dossier d’expert détaillera les conséquences et les stratégies de gestion de la SARA.
Qu'est-ce que l'acidose ruminale subclinique ?
L’acidose ruminale subclinique (SARA) est l’un des principaux problèmes nutritionnels chez les vaches laitières. Ce trouble métabolique entraîne une altération des fermentations ruminales causée par une transition alimentaire inadéquate et/ou une composition alimentaire inadaptée. Résultant d’un déséquilibre de la microflore ruminale causé par un régime riche en glucides fermentescibles et/ou pauvre en protéines, la SARA représente une menace permanente pour les ruminants à fort niveau de production.
Le pH optimal du rumen pour les vaches laitières hautes productrices se situe entre 6 et 6,5, permettant ainsi un bon équilibre de la microflore ruminale. Cependant, en raison des stratégies alimentaires intensives, des fluctuations quotidiennes du pH ruminal sont observées, induisant de manière irréversible une dégradation des papilles ruminales et une diminution de la capacité d’absorption des nutriments (Figure 1). Par conséquent, ces fluctuations quotidiennes du pH ruminal dégradent la santé et les performances zootechniques des animaux.
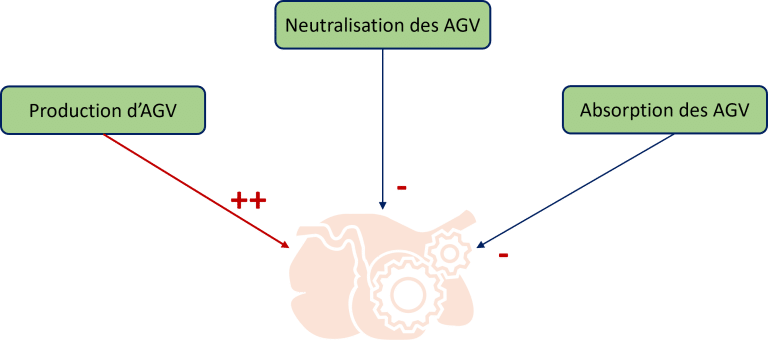
Figure 1 : Origine de l’acidose subclinique
L’acidose du rumen peut être définie comme une baisse du pH ruminal suite à la surproduction d’acides, en particulier d’acides gras volatils (AGV), par rapport à leurs neutralisation et absorption. Il existe deux formes d’acidose ruminale : l’acidose aiguë et l’acidose subclinique ou subaiguë (Sauvant, Reverdin, et Meschy, 2006). C’est cette dernière qui est développée ici.
La SARA est la conséquence d'un déséquilibre énergie/protéine dans l'alimentation
Les micro-organismes du rumen sont très sensibles aux fluctuations quotidiennes du pH. Pour optimiser les performances grâce à une densification énergétique de l’alimentation, les vaches sont en permanence à la limite de la SARA. Selon Plaizier et al. (2008), la SARA peut être décrite par un pH ruminal moyen inférieur à 5,6, pendant plus de 3,5 heures par jour. En effet, lorsque le pH ruminal descend en dessous de 6, l’activité cellulolytique, diminue alors que l’activité amylolytique augmente (Figure 2). Le rumen ne fonctionne plus correctement : les fermentations ruminales sont réduites. Comme les bactéries cellulolytiques permettent de digérer les fibres de l’alimentation, la digestion devient incomplète. C’est un cercle vicieux, car si ce déséquilibre n’est pas corrigé rapidement, les activités enzymatiques des Lactobacilles (adeptes des pH bas) continuent d’augmenter, induisant une augmentation de la production d’acide lactique et une diminution importante du pH ruminal. Les fermentations dans le rumen continuent de ralentir jusqu’à s’arrêter complètement, et les conséquences (technico-économiques) peuvent être considérables.
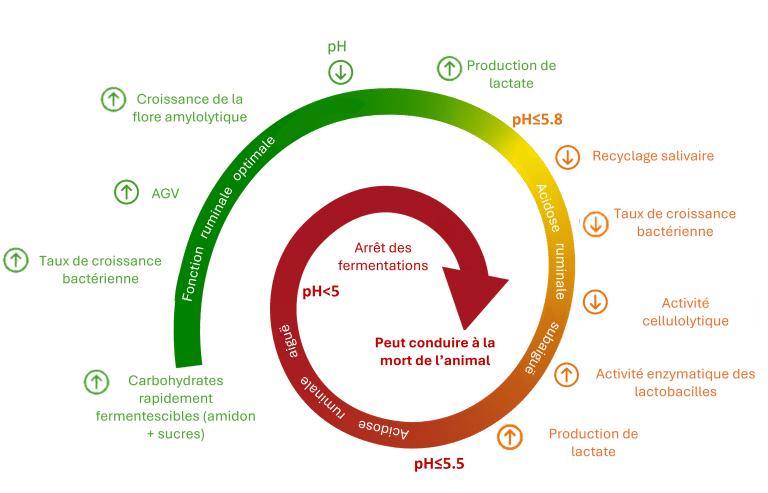
Figure 2 : Cercle vicieux de l’acidose. Adapté de Hernandez et al., 2014
Transition alimentaire : une période à haut risque pour les vaches
Les variations naturelles des silos de maïs ou d’herbe au fil du temps mettent à l’épreuve la stabilité de l’alimentation. En effet, l’ensilage de maïs continue d’évoluer quelques semaines après son ensilage. L’ensilage de maïs issu d’une seule récolte peut présenter des variations hebdomadaires dans ses valeurs nutritionnelles (par exemple, teneur en sucre, digestibilité de l’amidon, teneur en matière sèche, …). Cependant, avec les faibles rendements obtenus ces dernières années en raison de la sécheresse, il devient de plus en plus difficile de laisser fermenter l’ensilage de maïs pendant 1 à 3 mois avant de l’entamer. C’est pourquoi les vaches sont nourries avec des fourrages frais pouvant provoquer des troubles digestifs. Comparés aux fourrages conservées, les fourrages frais n’ont pas le temps de fermenter, ce qui augmente le risque de SARA chez l’animal. Ensuite, En effet, l’ensilage frais est riche en sucres rapidement fermentescibles. Une fois dans le rumen, ces sucres provoquent des fermentations rapides et déséquilibrées. La flore amylolytique est surstimulée, produisant principalement de fortes quantités d’AGV, principalement propionate et butyrate. Comme expliqué précédemment, cette forte production d’AGV dépasse le taux d’absorption par la paroi ruminale et la neutralisation par la salive, augmentant ainsi le risque de SARA.
Des difficultés similaires surviennent avec l’herbe de printemps et d’automne. En effet, l’herbe jeune est très riche en glucides rapidement fermentescibles (amidon et sucres), en azote et pauvre en fibres. Très agréable au goût pour les animaux, elle est consommée rapidement, ce qui diminue la salivation et augmente le risque de SARA. En raison de sa forte teneur en bicarbonate de sodium (12,5 g/L selon Erdman, (1988)), la salive constitue un tampon naturel pour le pH ruminal. Ainsi, une production de salive réduite signifie moins d’effet tampon sur le rumen.
Des niveaux d’amidon élevés et la source de cet amidon augmentent le risque de SARA
La composition de l’alimentation est un facteur clé dans la gestion de la SARA. Par exemple, la teneur en amidon mais aussi son origine peuvent augmenter le risque de SARA. Elmhadi et al. (2022), affirment qu’une teneur en amidon comprise entre 50 % et 65 % peut induire de la SARA. Khorrami et al. (2021), confirment que le temps passé avec un pH ruminal bas (< 6) augmente avec la teneur en amidon de l’alimentation. Ils ont également identifié que le type d’amidon utilisé peut influencer le risque de SARA. L’amidon de maïs est plus acidogène que l’orge et le blé s’il est distribué en grande quantité (> 20 % de la matière sèche totale ; Khorrami et al., 2021).
Comment détecter la SARA ?
Les conséquences de la SARA peuvent être nombreuses et varier d’un animal à l’autre. Elles peuvent se manifester sous la forme d’une ou plusieurs des observations visuelles listées dans la Figure 3.
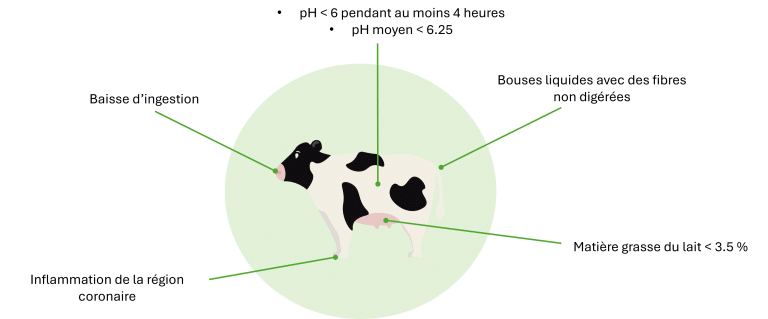
Figure 3 : Comment reconnaître la SARA chez les animaux ?
En réduisant la matière sèche ingérée (MSI ; -2,3 kg/jour en moyenne avec la SARA) et en impactant l’activité du rumen, la SARA conduit à une diminution de la production laitière, pouvant passer de 1,8 kg/jour à 3,3 kg/jour selon Chiquette et al. (2015). Outre cette perte de production, la diminution de l’activité des bactéries cellulolytiques impacte la teneur en matière grasse du lait via à une production plus faible d’acétate, un AGV précurseur de matière grasse. Chiquette et al. (2015) ont observé une diminution de 0,18 % du pourcentage de matière grasse du lait lors d’un challenge de SARA.
Chez les jeunes animaux, la SARA est également associée à une réduction de la MSI et du gain de poids moyen chez des veaux avant le sevrage (Wenli Li et al., 2019).
De plus, la SARA peut indirectement affecter les performances de reproduction. En effet, une efficacité alimentaire plus faible peut entraîner une note d’état corporel insuffisante qui affecte la reproduction. Comme le montrent Seesupa et al. (2017), la SARA peut également modifier le système hormonal, entraînant une fertilité plus faible.
Compte tenu de tout cela, la SARA représente un coût pour l’éleveur qui peut perdre environ 1,12 à 1,2€/vache/jour (Plaizier et al., 2008).
Comment limiter le risque de SARA ?
Pour réduire le risque de SARA, il est important de respecter les principes fondamentaux de la nutrition des ruminants :
- Effectuer des transitions alimentaires progressives
- Fournir suffisamment d’eau
- Assurez-vous d’une consommation régulière d’aliments tout au long de la journée
- Analysez le fourrage pour obtenir une alimentation équilibrée en énergie et en protéines
Le profil alimentaire en termes d’amidon et de fibres est également très important. En particulier, la teneur et la qualité de la fibre sont essentielles pour gérer le risque de SARA. Comme mentionné par Khorrami et al. (2021), les cas de SARA augmentent lorsque la teneur en amidon dépasse 20 % et que la peNDF > 8 (avec peNDF, la fibre détergente neutre physiquement efficace, c’est-à-dire ici, une taille de particule supérieure à 8 mm) est inférieure à 14 %. Néanmoins, la peNDF ne doit pas être trop élevée afin de ne pas limiter le MSI.
L’utilisation systématique ou ciblée pendant des périodes à risque de solutions tampons représente une stratégie clé pour soutenir les animaux et maintenir une activité ruminale optimale dans le cadre de la gestion de la SARA. Chez Phosphea, nous nous engageons à contribuer à limiter le risque de SARA en proposant notre solution tampon naturelle : Powder.
Comment CALSEA Power peut-il contribuer à la gestion de la SARA ?
CALSEA Powder est une solution naturelle basée à 100 % sur des algues marines calcaires (Lithothamnium calcareum). La structure poreuse de cette algue marine, combinée à sa structure cristalline unique, permet une forte solubilisation et une libération rapide d’ions calcium et carbonate dans le rumen, ce qui permet un meilleur maintien du pH ruminal.
Les vaches recevant le traitement bicarbonate de sodium (SBC ; 200 g/vache/jour) ont un pH ruminal moyen plus bas que celles avec le traitement CALSEA (100 g/vache/jour ; Figure 4). Le pH ruminal minimum obtenu avec le traitement SBC est de 5,45, ce qui est nettement inférieur au pH ruminal minimum obtenu avec CALSEA (Figure 4). De plus, avec CALSEA, le pourcentage d’animaux avec un pH ruminal < 5,5 est significativement inférieur à celui du SBC (Figure 4). Un pH < 6 pendant au moins 4 heures représente un risque d’acidose et, lorsque le pH est <5,5, ce risque est élevé. Selon les résultats, la capacité tampon de CALSEA est supérieure à celle du SBC.
CALSEA Powder agit comme une solution tampon favorisant la stabilité du pH ruminal, avec des effets positifs sur les populations microbiennes ruminales et un risque réduit de SARA. La figure 5 montre l’abondance relative de certaines bactéries indicatrices du statut de SARA avec différentes solutions tampons.
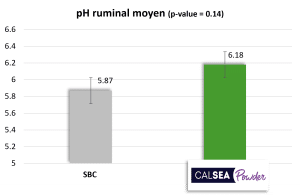
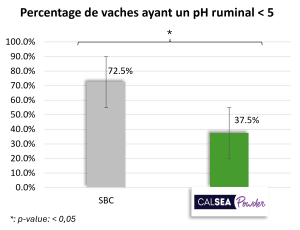
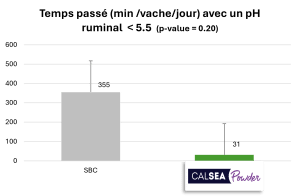
Figure 4 : Action du CALSEA Powder sur le pH ruminal comparé au bicarbonate de sodium (essai in vivo ; n=40).
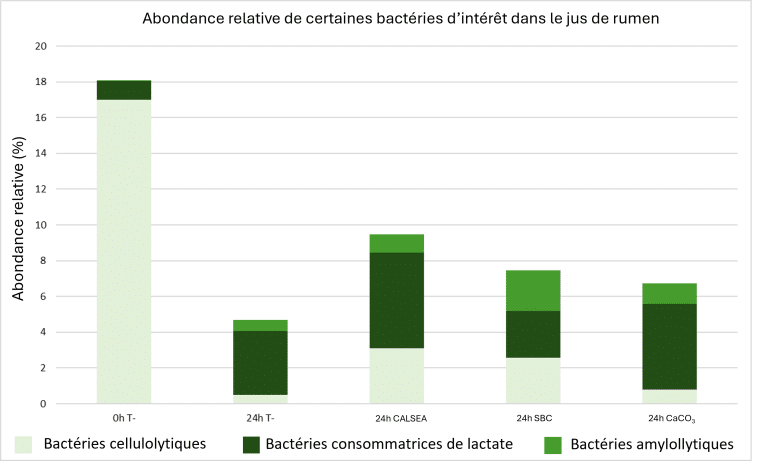
Figure 5 : Suivi in vitro des populations bactériennes ruminales en cas d’acidose ruminale subclinique (T- : Contrôle avec SARA)
0h T- représente le contrôle négatif sans tampon au temps 0. À ce stade, l’effet acidogène de l’alimentation n’est pas visible, la situation est considérée comme normale. Après 24 heures de fermentation sans tampon (24h T-), la SARA est installée et a négativement impacté les bactéries cellulolytiques, leur population a chuté drastiquement. Comparé au témoin négatif (T-24h), CALSEA (100 g/vache/jour) et SBC (200 g/vache/jour) semblent stimuler l’activité cellulolytique (Fibrobacter). Les bactéries consommatrices de lactate (Megasphaera) sont plus présentes avec CALSEA et CaCO3 qu’avec SBC. Cette dernière bactérie protège contre la SARA car elle consomme l’acide lactique. Cet essai montre que CALSEA favorise l’activité bactérienne cellulolytique dans des conditions acidogènes, contribuant ainsi à maintenir une efficacité ruminale optimale.
Products tailored to your livestock's need
Bibliographie
CHIQUETTE, J., LAGROST, J., GIRARD, C.L., TALBOT, G., LI, S., PLAIZIER, J.C. and HINDRICHSEN, I.K., 2015. Efficacy of the direct-fed microbial Enterococcus faecium alone or in combination with Saccharomyces cerevisiae or Lactococcus lactis during induced subacute ruminal acidosis. Journal of Dairy Science. January 2015. Vol. 98, n° 1, pp. 190‑203. DOI 10.3168/jds.2014-8219.
ELMHADI, Mawda E., ALI, Darien K., KHOGALI, Mawahib K. and WANG, Hongrong, 2022. Subacute ruminal acidosis in dairy herds: Microbiological and nutritional causes, consequences, and prevention strategies. Animal Nutrition. September 2022. Vol. 10, pp. 148‑155. DOI 10.1016/j.aninu.2021.12.008.
ENEMARK, Jörg M. D., 2008. The monitoring, prevention and treatment of sub-acute ruminal acidosis (SARA): A review. The Veterinary Journal. April 2008. Vol. 176, n° 1, pp. 32‑43. DOI 10.1016/j.tvjl.2007.12.021.
ERDMAN, Richard A., 1988. Dietary Buffering Requirements of the Lactating Dairy Cow: A Review1. Journal of Dairy Science. December 1988. Vol. 71, n° 12, pp. 3246‑3266. DOI 10.3168/jds.S0022-0302(88)79930-0.
FAOSTAT, [on line]. [Visited on January, 8th 2026]. Available on: https://www.fao.org/faostat/en/#data/QCL
KHORRAMI, Behzad, KHIAOSA-ARD, Ratchaneewan and ZEBELI, Qendrim, 2021. Models to predict the risk of subacute ruminal acidosis in dairy cows based on dietary and cow factors: A meta-analysis. Journal of Dairy Science. July 2021. Vol. 104, n° 7, pp. 7761‑7780. DOI 10.3168/jds.2020-19890.
KLEEN, J. L., HOOIJER, G. A., REHAGE, J. and NOORDHUIZEN, J. P. T. M., 2003. Subacute Ruminal Acidosis (SARA): a Review. Journal of Veterinary Medicine Series A. 2003. Vol. 50, n° 8, pp. 406‑414. DOI 10.1046/j.1439-0442.2003.00569.x.
LI, Wenli, GELSINGER, Sonia, EDWARDS, Andrea, RIEHLE, Christina and KOCH, Daniel, 2019. Transcriptome analysis of rumen epithelium and meta-transcriptome analysis of rumen epimural microbial community in young calves with feed induced acidosis. Scientific Reports. March 2019. Vol. 9, pp. 4744. DOI 10.1038/s41598-019-40375-2.
PLAIZIER, J. C., KRAUSE, D. O., GOZHO, G. N. and MCBRIDE, B. W., 2008. Subacute ruminal acidosis in dairy cows: The physiological causes, incidence and consequences. The Veterinary Journal. April 2008. Vol. 176, n° 1, pp. 21‑31. DOI 10.1016/j.tvjl.2007.12.016.
SAUVANT, D., REVERDIN, Stéphane et MESCHY, François, 2006. Le contrôle de l’acidose ruminale latente. INRA Productions Animales. 2006. Vol. 19, n° 2, pp. 69‑78.
